Mi lenne, ha mesterséges intelligencia segítségével megválaszolhatnánk az élet egyik legnagyobb titkát – a fehérje hajtogatását? A tudósok évtizedek óta dolgoznak ezen.
A gépek ma már elképesztő pontossággal megjósolhatják a fehérjeszerkezeteket a mélytanulási modellek segítségével, megváltoztatva a gyógyszerfejlesztést, a biotechnológiát és az alapvető biológiai folyamatokkal kapcsolatos ismereteinket.
Csatlakozzon hozzám, és fedezze fel a mesterséges intelligencia fehérje hajtogatásának izgalmas birodalmát, ahol a legmodernebb technológia ütközik magának az élet bonyolultságával.
A fehérjehajtogatás titkának megfejtése
A fehérjék kis gépekként működnek testünkben, hogy olyan kulcsfontosságú feladatokat hajtsanak végre, mint az élelmiszer lebontása vagy az oxigén szállítása. A hatékony működéshez megfelelően össze kell hajtani őket, ahogy a kulcsot is megfelelően kell vágni ahhoz, hogy a zárba illeszkedjen. Amint a fehérje létrejön, egy nagyon bonyolult hajtogatási folyamat veszi kezdetét.
A fehérje feltekeredése az a folyamat, amelynek során hosszú aminosavláncok, a fehérje építőkövei háromdimenziós struktúrákká hajtódnak össze, amelyek meghatározzák a fehérje működését.
Vegyünk egy hosszú gyöngysort, amelyet pontos formába kell rendelni; ez történik, amikor egy fehérje felhajlik. A gyöngyöktől eltérően azonban az aminosavak egyedi tulajdonságokkal rendelkeznek, és különböző módokon kölcsönhatásba lépnek egymással, így a fehérje hajtogatása összetett és érzékeny folyamat.
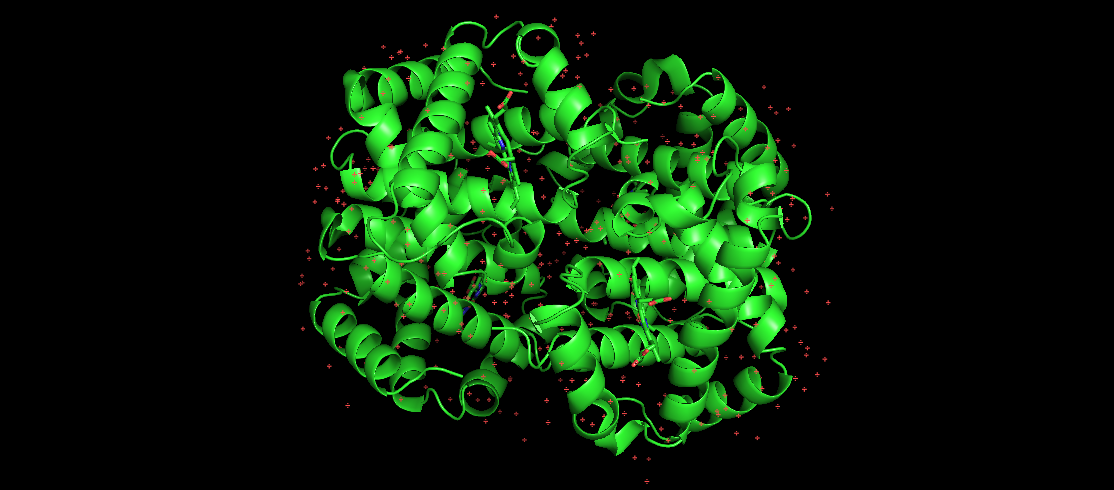
Az itt látható kép a humán hemoglobint ábrázolja, amely egy jól ismert hajtogatott fehérje
A fehérjéknek gyorsan és pontosan kell hajtogatniuk, különben rosszul hajtogatnak és hibásak lesznek. Ez olyan betegségekhez vezethet, mint az Alzheimer-kór és a Parkinson-kór. A hőmérséklet, a nyomás és más molekulák jelenléte a sejtben mind hatással van a hajtogatási folyamatra.
Több évtizedes kutatás után a tudósok még mindig próbálják kitalálni, hogy a fehérjék pontosan hogyan hajtogatnak.
Szerencsére a mesterséges intelligencia fejlődése javítja az ágazat fejlődését. A tudósok használatával minden eddiginél pontosabban megjósolhatják a fehérjék szerkezetét gépi tanulási algoritmusok hatalmas mennyiségű adat megvizsgálására.
Ez megváltoztathatja a gyógyszerfejlesztést, és növelheti a betegséggel kapcsolatos molekuláris tudásunkat.
Működhetnek jobban a gépek?
A hagyományos fehérjehajtogatási technikáknak korlátai vannak
A tudósok évtizedek óta próbálják kitalálni a fehérjehajtogatást, de a folyamat bonyolultsága miatt ez kihívást jelent.
A hagyományos fehérjeszerkezet-előrejelzési megközelítések a kísérleti módszerek és a számítógépes modellezés kombinációját alkalmazzák, azonban ezeknek a módszereknek vannak hátrányai.
Az olyan kísérleti technikák, mint a röntgenkrisztallográfia és a mágneses magrezonancia (NMR), időigényesek és költségesek lehetnek. A számítógépes modellek néha egyszerű feltételezésekre támaszkodnak, amelyek téves előrejelzésekhez vezethetnek.
A mesterséges intelligencia leküzdheti ezeket az akadályokat
Szerencsére, mesterséges intelligencia új ígéretet nyújt a pontosabb és hatékonyabb fehérjeszerkezet előrejelzéséhez. A gépi tanulási algoritmusok hatalmas mennyiségű adatot képesek megvizsgálni. És olyan mintákat tárnak fel, amelyeket az emberek hiányolnának.
Ennek eredményeként olyan új szoftvereszközök és platformok jöttek létre, amelyek páratlan pontossággal képesek előre jelezni a fehérje szerkezetét.
A legígéretesebb gépi tanulási algoritmusok a fehérjeszerkezet előrejelzéséhez
A Google által épített AlphaFold rendszer DeepMind csapat az egyik legígéretesebb előrelépés ezen a területen. Használata révén az elmúlt években nagy fejlődést ért el mély tanulási algoritmusok hogy megjósolják a fehérjék szerkezetét aminosavszekvenciáik alapján.
A neurális hálózatok, a támogató vektorgépek és a véletlenszerű erdők több olyan gépi tanulási módszer közé tartoznak, amelyek ígéretesek a fehérjeszerkezet előrejelzésében.
Ezek az algoritmusok hatalmas adatkészletekből tanulhatnak. És megjósolhatják a különböző aminosavak közötti összefüggéseket. Lássuk tehát, hogyan működik.

Ko-evolúciós elemzések és az első AlphaFold-generáció
A sikere AlphaFold mély neurális hálózati modellre épül, amelyet koevolúciós elemzéssel fejlesztettek ki. A koevolúció koncepciója kimondja, hogy ha egy fehérjében lévő két aminosav kölcsönhatásba lép egymással, akkor ezek együtt fejlődnek, hogy megtartsák funkcionális kapcsolatukat.
A kutatók számos hasonló fehérje aminosavszekvenciájának összehasonlításával kimutathatják, hogy a 3D-s szerkezetben valószínűleg mely aminosavpárok érintkeznek egymással.
Ezek az adatok szolgálnak az AlphaFold első iterációjának alapjául. Megjósolja az aminosavpárok közötti hosszokat, valamint az őket összekötő peptidkötések szögeit. Ez a módszer felülmúlta az összes korábbi megközelítést a fehérjeszerkezet szekvenciából történő előrejelzésére, bár a pontosság továbbra is korlátozott volt a nyilvánvaló templát nélküli fehérjék esetében.

AlphaFold 2: Egy radikálisan új módszertan
Az AlphaFold2 a DeepMind által létrehozott számítógépes szoftver, amely egy fehérje aminosavszekvenciáját használja a fehérje 3D szerkezetének előrejelzésére.
Ez azért fontos, mert a fehérje szerkezete határozza meg működését, és funkciójának megértése segíthet a tudósoknak olyan gyógyszerek kifejlesztésében, amelyek a fehérjét célozzák.
Az AlphaFold2 neurális hálózat bemenetként megkapja a fehérje aminosavszekvenciáját, valamint részleteket arról, hogy ez a szekvencia hogyan hasonlítható össze az adatbázisban lévő más szekvenciákkal (ezt nevezik „szekvencia-illesztésnek”).
A neurális hálózat e bemenet alapján jóslatot készít a fehérje 3D szerkezetére vonatkozóan.
Miben különbözik az AlphaFold2-től?
Más megközelítésekkel ellentétben az AlphaFold2 a fehérje valós 3D szerkezetét jósolja meg, nem pedig pusztán az aminosavpárok közötti elválasztást vagy az azokat összekötő kötések közötti szögeket (ahogyan a korábbi algoritmusok tették).
Annak érdekében, hogy a neurális hálózat azonnal megelőlegezze a teljes struktúrát, a struktúrát végpontok között kódolják.
Az AlphaFold2 másik fontos jellemzője, hogy becslést ad arra vonatkozóan, hogy mennyire biztos az előrejelzésében. Ez a várt szerkezet színkódjaként jelenik meg, a piros a magas, a kék pedig az alacsony megbízhatóságot.
Ez hasznos, mivel tájékoztatja a tudósokat az előrejelzés stabilitásáról.
Több szekvencia kombinált szerkezetének előrejelzése
Az Alphafold2 legújabb bővítése, az Alphafold Multimer néven ismert, több szekvencia kombinált szerkezetét jelzi előre. Még mindig magas a hibaaránya, még akkor is, ha sokkal jobban teljesít, mint a korábbi technikák. A 25 fehérjekomplexből mindössze 4500%-ot jósoltak meg sikeresen.
Az érintkezésképződés durva régióinak 70%-a helyesen volt megjósolva, de a két fehérje relatív orientációja helytelen volt. Ha a medián igazítási mélység kevesebb, mint nagyjából 30 szekvencia, az Alphafold multimer előrejelzések pontossága jelentősen csökken.
Az Alphafold előrejelzések használata
Az AlphaFold előrejelzett modelljei ugyanazokban a fájlformátumokban érhetők el, és ugyanúgy használhatók, mint a kísérleti struktúrák. A félreértések elkerülése érdekében kulcsfontosságú a modell által kínált pontossági becslések figyelembevétele.
Különösen hasznos olyan bonyolult szerkezeteknél, mint az összefonódott homomerek vagy fehérjék, amelyek csak egy
ismeretlen ligandum.
Néhány kihívás
Az előre jelzett struktúrák használatának fő problémája a dinamika, a ligandum szelektivitása, a kontroll, az allosztéria, a poszttranszlációs változások és a kötődés kinetikája megértése fehérje- és biofizikai adatokhoz való hozzáférés nélkül.
Gépi tanulás és a fizikán alapuló molekuladinamikai kutatások felhasználhatók e probléma leküzdésére.
Ezeknek a vizsgálatoknak előnyös lehet a speciális és hatékony számítógépes architektúra. Míg az AlphaFold óriási előrelépést ért el a fehérjeszerkezetek előrejelzésében, a szerkezetbiológia területén még mindig van mit tanulni, és az AlphaFold előrejelzései csak a kiindulópontot jelentik a jövőbeni tanulmányokhoz.
Mik az egyéb figyelemre méltó eszközök?
RoseTTAFold
A Washingtoni Egyetem kutatói által létrehozott RoseTTAFold szintén mély tanulási algoritmusokat alkalmaz a fehérjeszerkezetek előrejelzésére, de integrálja a „torziós szögdinamikai szimulációk” néven ismert új megközelítést is, hogy javítsa az előre jelzett struktúrákat.
Ez a módszer biztató eredményeket hozott, és hasznos lehet a meglévő mesterségesintelligencia-fehérje hajtogatási eszközök korlátainak leküzdésében.
trRosetta
Egy másik eszköz, a trRosetta, előrejelzi a fehérje feltekeredését az a neurális hálózat több millió fehérjeszekvencián és -struktúrán tanult.
Ezenkívül „templát alapú modellezési” technikát használ, hogy pontosabb előrejelzéseket készítsen a célfehérje összehasonlítható ismert struktúrákkal való összehasonlításával.
Kimutatták, hogy a trRosetta képes megjósolni apró fehérjék és fehérjekomplexek szerkezetét.
DeepMetaPSICOV
A DeepMetaPSICOV egy másik eszköz, amely a fehérjekontaktus-térképek előrejelzésére összpontosít. Ezeket útmutatóként használják a fehérje feltekeredésének előrejelzésére. Használja mély tanulás megközelítések a fehérjéken belüli maradék kölcsönhatások valószínűségének előrejelzésére.
Ezeket a későbbiekben a teljes kapcsolati térkép előrejelzésére használják. A DeepMetaPSICOV potenciált mutatott a fehérjeszerkezetek nagy pontosságú előrejelzésében, még akkor is, ha a korábbi megközelítések kudarcot vallottak.
Mit rejt a jövő?
Az AI fehérje hajtogatásának jövője fényes. A mély tanuláson alapuló algoritmusok, különösen az AlphaFold2, a közelmúltban nagy előrelépést értek el a fehérjeszerkezetek megbízható előrejelzésében.
Ez a felfedezés megváltoztathatja a gyógyszerfejlesztést azáltal, hogy lehetővé teszi a tudósok számára, hogy jobban megértsék a fehérjék szerkezetét és működését, amelyek általános terápiás célpontok.
Mindazonáltal továbbra is fennállnak olyan problémák, mint a fehérjekomplexek előrejelzése és a várható struktúrák valós funkcionális állapotának kimutatása. Több kutatásra van szükség ezeknek a problémáknak a megoldásához, valamint az AI-fehérje hajtogatási algoritmusok pontosságának és megbízhatóságának növeléséhez.
Ennek a technológiának a potenciális előnyei azonban óriásiak, és hatékonyabb és pontosabb gyógyszerek előállításához vezethet.





Hagy egy Válaszol