Forskare avslöjar de dolda strukturerna hos material och biomolekyler med hjälp av kristallografi och kryo-elektronmikroskopi (kryo-EM). Men eftersom dessa discipliner står inför ständigt ökande komplikationer, har maskininlärning blivit en värdefull allierad.
I det här inlägget kommer vi att titta på den fascinerande skärningspunkten mellan "Methods of Machine Learning for Crystallography and Cryo-EM." Följ med oss när vi undersöker den revolutionerande effekten av artificiell intelligens för att avslöja hemligheterna i atom- och molekyluniversum.
Först och främst vill jag lätta in på ämnet och nämna vad exakt är termerna för kristallografi och Cryo-Em, sedan ska vi undersöka ytterligare var maskininlärning kommer in i pjäsen.
Kristallografi
Kristallografi är studiet av arrangemanget av atomer i kristallina material. Kristaller är fasta ämnen som består av atomer som är ordnade i ett upprepande mönster för att bilda en mycket strukturerad struktur.
På grund av detta regelbundna arrangemang har material unika egenskaper och beteenden, vilket gör kristallografi avgörande för att förstå egenskaperna hos många ämnen.
Forskare kan undersöka kristallgittret med hjälp av tekniker som röntgendiffraktion, vilket ger viktig information om atompositioner och bindningsinteraktioner. Kristallografi är viktigt inom många områden, från materialvetenskap och kemi till geologi och biologi. Det hjälper till med utvecklingen av nya material och förståelsen av mineralegenskaper.
Det kan till och med hjälpa oss att dechiffrera de komplicerade strukturerna hos biologiska molekyler som proteiner.
Cryo-EM (Cryo-Electron Microscopy)
Kryoelektronmikroskopi (Cryo-EM) är en sofistikerad bildteknik som gör det möjligt för forskare att se de tredimensionella strukturerna hos biomolekyler i atomär eller nära atomär upplösning.
Cryo-EM bevarar biomolekyler i deras nästan naturliga tillstånd genom att snabbt frysa dem i flytande kväve, i motsats till standard elektronmikroskopi, som kräver att prover fixeras, färgas och dehydreras.
Detta förhindrar iskristallbildning och bevarar den biologiska strukturen. Forskare kan nu se exakta detaljer om enorma proteinkomplex, virus och cellulära organeller, vilket ger avgörande insikter om deras funktioner och relationer.
Cryo-EM har förändrat strukturbiologin genom att tillåta forskare att utforska biologiska processer på tidigare otänkbara detaljnivåer. Dess tillämpningar sträcker sig från läkemedelsupptäckt och vaccinutveckling till att förstå sjukdomsmolekylära grunder.
Varför är de viktiga?
Kryo-EM och kristallografi är avgörande för att främja vår förståelse av den naturliga världen.
Kristallografi gör det möjligt för oss att upptäcka och förstå atomarrangemanget i material, vilket gör att vi kan bygga nya föreningar med specifika egenskaper för ett brett spektrum av användningsområden. Kristallografi är avgörande för att forma vår moderna kultur, från halvledare som används i elektronik till mediciner som används för att behandla åkommor.
Cryo-EM, å andra sidan, ger en fascinerande inblick i livets komplicerade mekanism. Forskare skaffar sig insikter i grundläggande biologiska processer genom att se biomolekylernas arkitektur, vilket gör att de kan producera bättre mediciner, designa riktade terapier och effektivt bekämpa infektionssjukdomar.
Cryo-EM-framsteg öppnar för nya vyer inom medicin, bioteknik och vår övergripande förståelse av livets byggstenar.
Förbättra strukturförutsägelse och analys med maskininlärning i kristallografi
Maskininlärning har varit oerhört hjälpsam inom kristallografi, och revolutionerat hur forskare förutsäger och tolkar kristallstrukturer.
Algoritmer kan extrahera mönster och korrelationer från enorma datamängder av kända kristallstrukturer, vilket möjliggör snabb förutsägelse av nya kristallstrukturer med oöverträffad precision.
Thorn Labs forskare har till exempel bevisat effektiviteten hos maskininlärning när det gäller att förutsäga kristallstabilitet och formationsenergi, vilket ger viktiga insikter om materialens termodynamiska egenskaper.
Denna utveckling påskyndar inte bara upptäckten av nya material utan också optimeringen av nuvarande, vilket leder till en ny era av materialforskning med bättre kvaliteter och funktionalitet.
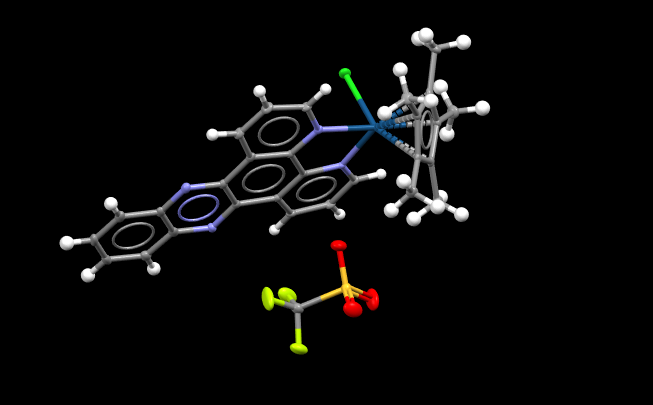
Bild: Ett exempel på en kristallstruktur illustrerad på Mercury-programvaran.
Hur avslöjar Machine Learning Cryo-EM?
Maskininlärning har öppnat upp en ny värld av möjligheter inom kryoelektronmikroskopi (Cryo-EM), vilket gör att forskare kan fördjupa sig djupare i biomolekylernas strukturella komplexitet.
Forskare kan analysera enorma volymer av kryo-EM-data med hjälp av nya teknologier som t.ex djupt lärande, rekonstruerar tredimensionella modeller av biologiska molekyler med oöverträffad tydlighet och noggrannhet.
Denna kombination av maskininlärning med cryo-EM har möjliggjort avbildning av tidigare otydliga proteinstrukturer, vilket ger nya insikter om deras aktiviteter och relationer.
Kombinationen av dessa teknologier har ett enormt löfte för läkemedelsupptäckten eftersom det gör det möjligt för forskare att exakt rikta in sig på specifika bindningsställen, vilket leder till skapandet av mer effektiva läkemedel för en mängd olika sjukdomar.
Machine Learning Algoritmer för att accelerera Cryo-EM-dataanalys
Cryo-EM-undersökningar genererar detaljerade och massiva datamängder, som kan vara både en gåva och en förbannelse för forskare. Maskininlärningsmetoder har dock visat sig vara avgörande för effektiv analys och tolkning av kryo-EM-data.
Forskare kan använda oövervakade inlärningsmetoder för att automatiskt upptäcka och klassificera olika proteinstrukturer, vilket minskar de tidskrävande manuella operationerna.
Denna metod påskyndar inte bara dataanalysen utan förbättrar också resultatens pålitlighet genom att ta bort mänskliga fördomar i tolkningen av komplicerade strukturella data.
Införandet av maskininlärning i Cryo-EM-dataanalys, som visats i senare arbeten, erbjuder ett sätt för en djupare kunskap om komplicerade biologiska processer och en mer grundlig undersökning av livets molekylära maskineri.
Mot hybrida tillvägagångssätt: Överbrygga gapet mellan experiment och beräkning
Maskininlärning har potential att överbrygga gapet mellan experimentella data och beräkningsmodeller inom kristallografi och kryo-EM.
Kombinationen av experimentella data och maskininlärningstekniker möjliggör utvecklingen av exakta prediktiva modeller, vilket förbättrar tillförlitligheten för strukturbestämning och egenskapsuppskattning.
Transfer learning, en teknik som tillämpar kunskap som lärts inom ett område till ett annat, framstår som ett viktigt verktyg för att öka effektiviteten av kristallografiska och Cryo-EM-undersökningar i detta sammanhang.
Hybridtekniker, som kombinerar experimentella insikter med datorkapacitet, representerar ett banbrytande alternativ för att lösa utmanande vetenskapliga utmaningar, och lovar att förändra hur vi ser och manipulerar den atomära och molekylära världen.
Använda konvolutionella neurala nätverk för att plocka partiklar i Cryo-EM
Genom att ge högupplösta bilder av biologiska molekyler har kryo-elektronmikroskopi (Cryo-EM) förändrat studiet av makromolekylära strukturer.
Men partikelplockning, som innebär att känna igen och extrahera enskilda partikelbilder från Cryo-EM-mikrografer, har varit en tidskrävande och mödosam uppgift.
Forskare har gjort enorma framsteg i att automatisera denna procedur med användning av maskininlärning, särskilt convolutional neurala nätverk (CNN).
DeepPicker och Topaz-Denoise är två djupa inlärningsalgoritmer som möjliggör helautomatiskt partikelval i cryo-EM, vilket avsevärt påskyndar databearbetning och analys.
CNN-baserade tillvägagångssätt har blivit avgörande för att påskynda Cryo-EM-procedurer och tillåta forskare att fokusera på undersökningar på högre nivå genom att noggrant detektera partiklar med hög precision.
Optimering av kristallografi med hjälp av prediktiv modellering
Kvaliteten på diffraktionsdata och kristallisationsresultat kan ha en betydande inverkan på strukturbestämningen i makromolekylär kristallografi.
Artificiella neurala nätverk (ANN) och stödvektormaskiner (SVM) har använts framgångsrikt för att optimera kristalliseringsinställningar och förutsäga kristalldiffraktionskvalitet. Prediktiva modeller framtagna av forskare hjälper till med designen av experiment och ökar framgångsfrekvensen för kristalliseringsförsök.
Dessa modeller kan avslöja mönster som leder till goda resultat genom att utvärdera enorma volymer av kristallisationsdata, vilket hjälper forskare att producera högkvalitativa kristaller för efterföljande röntgendiffraktionstester. Som ett resultat har maskininlärning blivit ett oumbärligt verktyg för snabba och målinriktade kristallografiska tester.
Förbättra Cryo-EM strukturell igenkänning
Att förstå den sekundära strukturen hos biologiska molekyler med Cryo-EM-densitetskartor är avgörande för att bestämma deras funktioner och interaktioner.
Tillvägagångssätt för maskininlärning, nämligen djupinlärningsarkitekturer såsom graffalsning och återkommande nätverk, har använts för att lokalisera sekundära strukturfunktioner i cryo-EM-kartor automatiskt.
Dessa metoder undersöker lokala egenskaper i densitetskartor, vilket möjliggör exakt klassificering av sekundära strukturella element. Maskininlärning gör det möjligt för forskare att undersöka komplicerade kemiska strukturer och få insikter i deras biologiska aktiviteter genom att automatisera denna arbetsintensiva process.

Bild: Cryo-EM-rekonstitution av en struktur
Kristallografisk modellbyggnad och valideringsacceleration
Modellkonstruktion och validering är nyckelfaser i makromolekylär kristallografi för att säkerställa strukturell modell noggrannhet och tillförlitlighet.
Maskininlärningsteknologier som faltningsautokodare och Bayesianska modeller har använts för att underlätta och förbättra dessa processer. AAnchor, till exempel, använder CNN för att känna igen ankaraminosyror i Cryo-EM-densitetskartor, vilket hjälper till med automatisk modellutveckling.
Bayesianska maskininlärningsmodeller användes också för att integrera röntgendiffraktionsdata och tilldela rymdgrupper i elektrondensitetskartor för små molekyler.
Dessa framsteg påskyndar inte bara strukturbestämningen utan ger också mer omfattande bedömningar av modellkvalitet, vilket resulterar i mer robusta och reproducerbara forskningsresultat.
Maskinlärandes framtid inom strukturbiologi
Som framgår av det växande antalet vetenskapliga publikationer, förbättras integreringen av maskininlärning i kryo-EM och kristallografi ständigt, vilket ger en uppsjö av nya lösningar och applikationer.
Maskininlärning lovar att ytterligare förvandla den strukturella biologimiljön med den kontinuerliga utvecklingen av kraftfulla algoritmer och utbyggnaden av kurerade resurser.
Synergin mellan maskininlärning och strukturbiologi banar väg för upptäckter och insikter i den atomära och molekylära världen, från snabb strukturbestämning till läkemedelsupptäckt och proteinteknik.
Den pågående forskningen om detta fascinerande ämne inspirerar forskare att utnyttja kraften i AI och låsa upp mysterierna med livets byggstenar.
Slutsats
Införlivandet av maskininlärningsteknologier i kristallografi och kryoelektronmikroskopi har öppnat en ny tid inom strukturbiologin.
Maskininlärning har avsevärt påskyndat forskningstakten och gett oöverträffade insikter i atom- och molekylvärlden, från automatisering av svåra operationer som partikelurval till att förbättra prediktiv modellering för kristallisation och diffraktionskvalitet.
Forskare kan nu effektivt utvärdera enorma mängder data med hjälp av faltning neurala nätverk och andra avancerade algoritmer, som omedelbart förutser kristallstrukturer och extraherar värdefull information från densitetskartor för kryo-elektronmikroskopi.
Denna utveckling påskyndar inte bara experimentella operationer utan möjliggör också en mer djupgående studie av biologiska strukturer och funktioner.
Slutligen förändrar konvergensen av maskininlärning och strukturell biologi landskapet för kristallografi och kryo-elektronmikroskopi.
Tillsammans för dessa spjutspetsteknologier oss närmare en bättre förståelse av atom- och molekylvärlden, och lovar genombrott som förändrar spelet inom materialforskning, läkemedelsutveckling och livets invecklade maskineri.
När vi omfamnar denna fascinerande nya gräns, lyser framtiden för strukturbiologin ljust med gränslösa möjligheter och förmågan att lösa naturens svåraste pussel.





Kommentera uppropet