Wetenschappers onthullen de verborgen structuren van materialen en biomoleculen met behulp van kristallografie en cryo-elektronenmicroscopie (cryo-EM). Omdat deze disciplines echter met steeds grotere complicaties worden geconfronteerd, is machine learning een waardevolle bondgenoot geworden.
In dit bericht kijken we naar de fascinerende kruising van "Methods of Machine Learning for Crystallography and Cryo-EM." Ga met ons mee terwijl we de revolutionaire impact van kunstmatige intelligentie onderzoeken bij het ontsluiten van de geheimen van de atomaire en moleculaire universums.
Allereerst wil ik het onderwerp verlichten en vermelden wat precies de termen van kristallografie en Cryo-Em zijn, daarna zullen we verder onderzoeken waar machine learning komt in het spel.
kristallografie
Kristallografie is de studie van de rangschikking van atomen in kristallijne materialen. Kristallen zijn vaste stoffen die zijn opgebouwd uit atomen die in een zich herhalend patroon zijn gerangschikt om een zeer gestructureerde structuur te vormen.
Vanwege deze regelmatige opstelling hebben materialen unieke eigenschappen en gedragingen, waardoor kristallografie van vitaal belang is voor het begrijpen van de eigenschappen van veel stoffen.
Wetenschappers kunnen het kristalrooster onderzoeken met behulp van technieken zoals röntgendiffractie, waardoor cruciale informatie wordt verkregen over atoomposities en bindingsinteracties. Kristallografie is belangrijk op veel gebieden, van materiaalkunde en scheikunde tot geologie en biologie. Het helpt bij de ontwikkeling van nieuwe materialen en het begrijpen van minerale eigenschappen.
Het kan ons zelfs helpen bij het ontcijferen van de ingewikkelde structuren van biologische moleculen zoals eiwitten.
Cryo-EM (Cryo-elektronenmicroscopie)
Cryo-elektronenmicroscopie (Cryo-EM) is een geavanceerde beeldvormingstechnologie waarmee onderzoekers de driedimensionale structuren van biomoleculen met atomaire of bijna atomaire resolutie kunnen zien.
Cryo-EM bewaart biomoleculen in hun bijna natuurlijke staat door ze snel in vloeibare stikstof te bevriezen, in tegenstelling tot standaard elektronenmicroscopie, waarbij monsters moeten worden gefixeerd, gekleurd en gedehydrateerd.
Dit voorkomt de vorming van ijskristallen, waardoor de biologische structuur behouden blijft. Wetenschappers kunnen nu nauwkeurige details zien van enorme eiwitcomplexen, virussen en cellulaire organellen, wat cruciale inzichten verschaft in hun functies en relaties.
Cryo-EM heeft de structurele biologie getransformeerd door onderzoekers in staat te stellen biologische processen te onderzoeken op voorheen ondenkbare detailniveaus. De toepassingen variëren van de ontdekking van geneesmiddelen en de ontwikkeling van vaccins tot het begrijpen van de moleculaire grondslagen van ziekten.
Waarom zijn ze belangrijk?
Cryo-EM en kristallografie zijn cruciaal om ons begrip van de natuurlijke wereld te vergroten.
Kristallografie stelt ons in staat om de atomaire rangschikking in materialen te ontdekken en te begrijpen, waardoor we nieuwe verbindingen kunnen bouwen met specifieke eigenschappen voor een breed scala aan toepassingen. Kristallografie is essentieel bij het vormgeven van onze moderne cultuur, van halfgeleiders die worden gebruikt in elektronica tot medicijnen die worden gebruikt om aandoeningen te behandelen.
Cryo-EM daarentegen geeft een fascinerende kijk op het gecompliceerde mechanisme van het leven. Wetenschappers verwerven inzicht in fundamentele biologische processen door de architectuur van biomoleculen te bekijken, waardoor ze betere medicijnen kunnen produceren, gerichte therapieën kunnen ontwerpen en infectieziekten efficiënt kunnen bestrijden.
Cryo-EM-vooruitgang opent nieuwe perspectieven in de geneeskunde, biotechnologie en ons algemene begrip van de bouwstenen van het leven.
Verbetering van structuurvoorspelling en -analyse met machine learning in kristallografie
Machine learning is ongelooflijk nuttig geweest bij kristallografie en heeft een revolutie teweeggebracht in de manier waarop wetenschappers kristalstructuren voorspellen en interpreteren.
Algoritmen kunnen patronen en correlaties extraheren uit enorme datasets van bekende kristalstructuren, waardoor nieuwe kristalstructuren snel kunnen worden voorspeld met een ongeëvenaarde precisie.
Onderzoekers van Thorn Lab hebben bijvoorbeeld de effectiviteit van machine learning bewezen bij het voorspellen van kristalstabiliteit en formatie-energie, waardoor essentiële inzichten in de thermodynamische eigenschappen van materialen worden verkregen.
Deze ontwikkeling versnelt niet alleen de ontdekking van nieuwe materialen, maar ook de optimalisatie van bestaande materialen, waarmee een nieuw tijdperk van materiaalonderzoek met betere kwaliteiten en functionaliteiten wordt ingeluid.
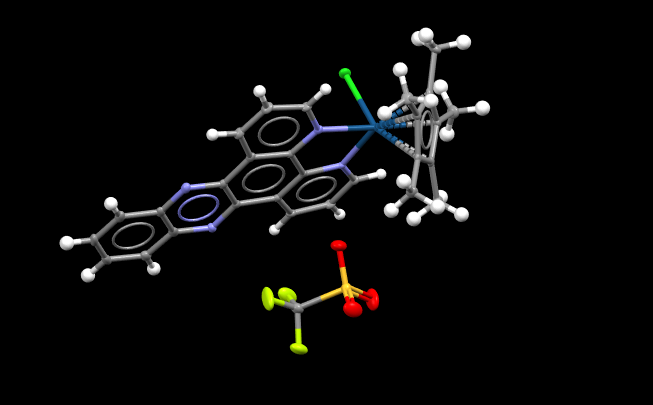
Afbeelding: een voorbeeld van een kristalstructuur geïllustreerd op Mercury-software.
Hoe machine learning de Cryo-EM onthult?
Machine learning heeft een nieuwe wereld van mogelijkheden geopend in cryo-elektronenmicroscopie (Cryo-EM), waardoor wetenschappers dieper kunnen graven in de structurele complexiteit van biomoleculen.
Onderzoekers kunnen enorme hoeveelheden cryo-EM-gegevens analyseren met behulp van nieuwe technologieën zoals diepgaand leren, driedimensionale modellen van biologische moleculen reconstrueren met ongeëvenaarde helderheid en nauwkeurigheid.
Deze combinatie van machinaal leren met cryo-EM heeft het mogelijk gemaakt om voorheen onontcijferbare eiwitstructuren in beeld te brengen, wat nieuwe inzichten in hun activiteiten en relaties opleverde.
De combinatie van deze technologieën houdt een enorme belofte in voor de ontdekking van geneesmiddelen, omdat onderzoekers hierdoor nauwkeurig op specifieke bindingsplaatsen kunnen worden gericht, wat leidt tot de creatie van effectievere geneesmiddelen voor een verscheidenheid aan aandoeningen.
Machine Learning-algoritmen voor het versnellen van Cryo-EM-gegevensanalyse
Cryo-EM-onderzoeken genereren gedetailleerde en enorme datasets, die zowel een geschenk als een vloek kunnen zijn voor onderzoekers. Methoden voor machinaal leren zijn echter essentieel gebleken bij de effectieve analyse en interpretatie van cryo-EM-gegevens.
Wetenschappers kunnen leerbenaderingen zonder toezicht gebruiken om verschillende eiwitstructuren automatisch te detecteren en te classificeren, waardoor tijdrovende handmatige handelingen worden verminderd.
Deze methode versnelt niet alleen de gegevensanalyse, maar verbetert ook de betrouwbaarheid van de bevindingen door menselijke vooroordelen bij de interpretatie van ingewikkelde structurele gegevens weg te nemen.
De integratie van machine learning in Cryo-EM-gegevensanalyse, zoals aangetoond in recente werken, biedt een manier voor een diepere kennis van gecompliceerde biologische processen en een grondiger onderzoek van de moleculaire machinerie van het leven.
Op weg naar hybride benaderingen: de experiment-rekenkloof overbruggen
Machine learning heeft het potentieel om de kloof tussen experimentele gegevens en computermodellen in kristallografie en cryo-EM te overbruggen.
De combinatie van experimentele gegevens en machine learning-technieken maakt de ontwikkeling van nauwkeurige voorspellende modellen mogelijk, waardoor de betrouwbaarheid van structuurbepaling en eigendomsschatting wordt verbeterd.
Transfer learning, een techniek die kennis die op het ene gebied is opgedaan, toepast op een ander, lijkt in deze context een belangrijk hulpmiddel te zijn om de efficiëntie van kristallografische en Cryo-EM-onderzoeken te vergroten.
Hybride technieken, die experimentele inzichten combineren met computercapaciteit, vormen een geavanceerde optie voor het oplossen van uitdagende wetenschappelijke uitdagingen en beloven de manier waarop we de atomaire en moleculaire wereld zien en manipuleren te veranderen.
Convolutionele neurale netwerken gebruiken om deeltjes in Cryo-EM te kiezen
Door beelden met een hoge resolutie van biologische moleculen te geven, heeft cryo-elektronenmicroscopie (Cryo-EM) de studie van macromoleculaire structuren getransformeerd.
Het oppakken van deeltjes, waarbij afzonderlijke deeltjesbeelden uit Cryo-EM-microfoto's worden herkend en geëxtraheerd, is echter een tijdrovende en zware taak geweest.
Onderzoekers hebben enorme vooruitgang geboekt bij het automatiseren van deze procedure, vooral met behulp van machine learning convolutionele neurale netwerken (CNN's).
DeepPicker en Topaz-Denoise zijn twee diepe leeralgoritmen die volledig geautomatiseerde deeltjesselectie in cryo-EM mogelijk maken, waardoor gegevensverwerking en -analyse aanzienlijk worden versneld.
Op CNN gebaseerde benaderingen zijn van cruciaal belang geworden om Cryo-EM-procedures te versnellen en onderzoekers in staat te stellen zich te concentreren op onderzoek op hoger niveau door deeltjes nauwkeurig met hoge precisie te detecteren.
Optimalisatie van kristallografie met behulp van voorspellende modellering
De kwaliteit van diffractiegegevens en kristallisatieresultaten kan een aanzienlijke invloed hebben op de structuurbepaling in macromoleculaire kristallografie.
Kunstmatige neurale netwerken (ANN's) en ondersteunende vectormachines (SVM's) zijn met succes gebruikt om de kristallisatie-instellingen te optimaliseren en de kristaldiffractiekwaliteit te voorspellen. Voorspellende modellen die door onderzoekers zijn gemaakt, helpen bij het ontwerpen van experimenten en verhogen het slagingspercentage van kristallisatieproeven.
Deze modellen kunnen patronen ontdekken die tot goede resultaten leiden door enorme hoeveelheden kristallisatiegegevens te evalueren, en onderzoekers te helpen bij het produceren van hoogwaardige kristallen voor daaropvolgende röntgendiffractietests. Als gevolg hiervan is machine learning een onmisbaar hulpmiddel geworden voor snelle en gerichte kristallografische tests.
Verbetering van Cryo-EM structurele herkenning
Het begrijpen van de secundaire structuur van biologische moleculen met behulp van Cryo-EM-dichtheidskaarten is van cruciaal belang voor het bepalen van hun functies en interacties.
Machine learning-benaderingen, namelijk deep learning-architecturen zoals grafische convolutionele en terugkerende netwerken, zijn gebruikt om automatisch secundaire structuurkenmerken in cryo-EM-kaarten te lokaliseren.
Deze methoden onderzoeken lokale kenmerken in dichtheidskaarten, waardoor een nauwkeurige classificatie van secundaire structurele elementen mogelijk is. Machine learning stelt onderzoekers in staat ingewikkelde chemische structuren te onderzoeken en inzicht te verwerven in hun biologische activiteiten door dit arbeidsintensieve proces te automatiseren.

Afbeelding: Cryo-EM-reconstitutie van een structuur
Kristallografie Modelbouw en validatieversnelling
Modelconstructie en validatie zijn sleutelfasen in macromoleculaire kristallografie om de nauwkeurigheid en betrouwbaarheid van structurele modellen te verzekeren.
Machine learning-technologieën zoals convolutionele auto-encoders en Bayesiaanse modellen zijn gebruikt om deze processen te ondersteunen en te verbeteren. AAnchor gebruikt bijvoorbeeld CNN's om ankeraminozuren te herkennen in Cryo-EM-dichtheidskaarten, wat helpt bij automatische modelontwikkeling.
Bayesiaanse machine learning-modellen werden ook gebruikt om röntgendiffractiegegevens te integreren en ruimtegroepen toe te wijzen in elektronendichtheidskaarten met kleine moleculen.
Deze vorderingen versnellen niet alleen de structuurbepaling, maar bieden ook uitgebreidere beoordelingen van de modelkwaliteit, wat resulteert in meer robuuste en reproduceerbare onderzoeksoutputs.
De toekomst van machinaal leren in structurele biologie
Zoals blijkt uit het groeiende aantal wetenschappelijke publicaties, wordt de integratie van machine learning in cryo-EM en kristallografie voortdurend verbeterd, wat een overvloed aan nieuwe oplossingen en toepassingen oplevert.
Machine learning belooft de structurele biologische omgeving verder te transformeren met de voortdurende ontwikkeling van krachtige algoritmen en de uitbreiding van beheerde bronnen.
De synergie tussen machine learning en structurele biologie maakt de weg vrij voor ontdekkingen en inzichten in de atomaire en moleculaire wereld, van snelle structuurbepaling tot medicijnontdekking en eiwittechnologie.
Het lopende onderzoek naar dit fascinerende onderwerp inspireert wetenschappers om de kracht van AI te benutten en de mysteries van de bouwstenen van het leven te ontrafelen.
Conclusie
De integratie van machine learning-technologieën in kristallografie en cryo-elektronenmicroscopie heeft een nieuw tijdperk in structurele biologie geopend.
Machine learning heeft het onderzoekstempo aanzienlijk versneld en ongeëvenaarde inzichten in de atomaire en moleculaire wereld opgeleverd, van het automatiseren van zware operaties zoals deeltjesselectie tot het verbeteren van voorspellende modellering voor kristallisatie en diffractiekwaliteit.
Onderzoekers kunnen nu enorme hoeveelheden gegevens efficiënt evalueren met behulp van convolutie neurale netwerken en andere geavanceerde algoritmen, die onmiddellijk anticiperen op kristalstructuren en waardevolle informatie extraheren uit cryo-elektronenmicroscopiedichtheidskaarten.
Deze ontwikkelingen versnellen niet alleen experimentele operaties, maar maken ook een meer diepgaande studie van biologische structuren en functies mogelijk.
Ten slotte verandert de convergentie van machine learning en structurele biologie de landschappen van kristallografie en cryo-elektronenmicroscopie.
Samen brengen deze geavanceerde technologieën ons dichter bij een beter begrip van de atomaire en moleculaire werelden, en beloven baanbrekende doorbraken in materiaalonderzoek, medicijnontwikkeling en de ingewikkelde machinerie van het leven zelf.
Terwijl we deze fascinerende nieuwe grens omarmen, schittert de toekomst van structurele biologie helder met grenzeloze mogelijkheden en het vermogen om de moeilijkste puzzels van de natuur op te lossen.





Laat een reactie achter