ജീവിതത്തിലെ ഏറ്റവും വലിയ നിഗൂഢതകളിലൊന്നായ പ്രോട്ടീൻ ഫോൾഡിംഗിന് ഉത്തരം നൽകാൻ നമുക്ക് കൃത്രിമബുദ്ധി ഉപയോഗിക്കാനായാലോ? പതിറ്റാണ്ടുകളായി ശാസ്ത്രജ്ഞർ ഇതിനായി പരിശ്രമിച്ചുകൊണ്ടിരിക്കുകയാണ്.
ആഴത്തിലുള്ള പഠന മാതൃകകൾ, മയക്കുമരുന്ന് വികസനം, ബയോടെക്നോളജി, അടിസ്ഥാന ജൈവ പ്രക്രിയകളെക്കുറിച്ചുള്ള നമ്മുടെ അറിവ് എന്നിവ ഉപയോഗിച്ച് യന്ത്രങ്ങൾക്ക് ഇപ്പോൾ പ്രോട്ടീൻ ഘടനകളെ അതിശയകരമായ കൃത്യതയോടെ പ്രവചിക്കാൻ കഴിയും.
അത്യാധുനിക സാങ്കേതികവിദ്യ ജീവിതത്തിന്റെ സങ്കീർണ്ണതയുമായി കൂട്ടിയിടിക്കുന്ന AI പ്രോട്ടീൻ ഫോൾഡിംഗിന്റെ കൗതുകകരമായ മണ്ഡലത്തിലേക്ക് ഒരു പര്യവേക്ഷണത്തിൽ എന്നോടൊപ്പം ചേരൂ.
പ്രോട്ടീൻ ഫോൾഡിംഗിന്റെ രഹസ്യം അനാവരണം ചെയ്യുന്നു
ഭക്ഷണം വിഘടിപ്പിക്കുന്നതോ ഓക്സിജൻ കടത്തിവിടുന്നതോ പോലുള്ള നിർണായക ജോലികൾ ചെയ്യാൻ ചെറിയ യന്ത്രങ്ങളെപ്പോലെ പ്രോട്ടീനുകൾ നമ്മുടെ ശരീരത്തിൽ പ്രവർത്തിക്കുന്നു. ഒരു പൂട്ടിൽ ഘടിപ്പിക്കുന്നതിന് ഒരു താക്കോൽ ശരിയായി മുറിക്കേണ്ടത് പോലെ, ഫലപ്രദമായി പ്രവർത്തിക്കുന്നതിന് അവ ശരിയായി മടക്കിയിരിക്കണം. പ്രോട്ടീൻ സൃഷ്ടിച്ച ഉടൻ, വളരെ സങ്കീർണ്ണമായ ഒരു മടക്കൽ പ്രക്രിയ ആരംഭിക്കുന്നു.
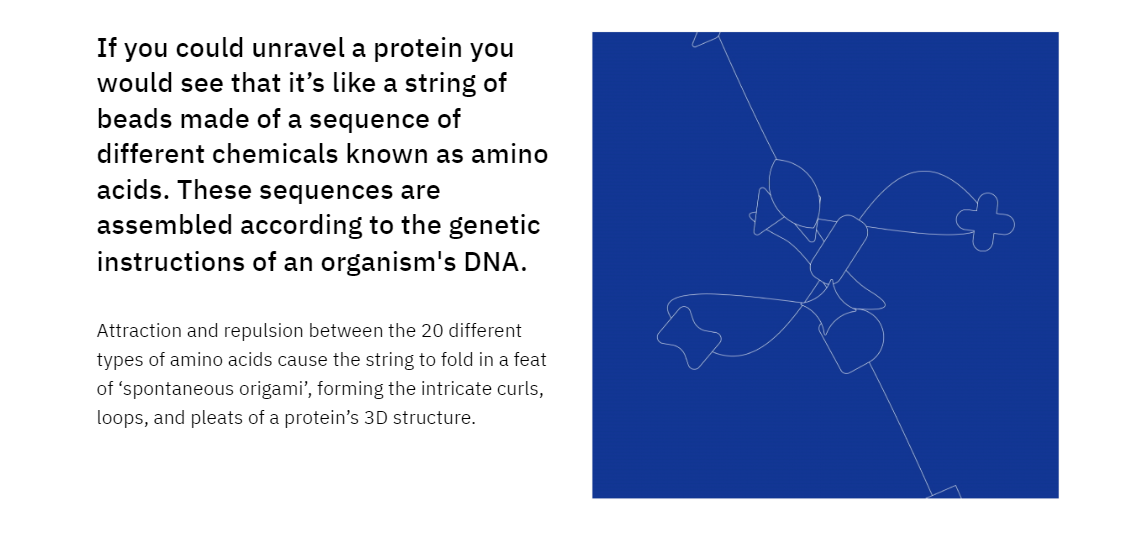
പ്രോട്ടീന്റെ നിർമ്മാണ ബ്ലോക്കുകളായ അമിനോ ആസിഡുകളുടെ ദൈർഘ്യമേറിയ ശൃംഖലകൾ പ്രോട്ടീന്റെ പ്രവർത്തനത്തെ നിർണ്ണയിക്കുന്ന ത്രിമാന ഘടനകളായി മടക്കിക്കളയുന്ന പ്രക്രിയയാണ് പ്രോട്ടീൻ ഫോൾഡിംഗ്.
കൃത്യമായ രൂപത്തിൽ ക്രമപ്പെടുത്തേണ്ട നീളമുള്ള മുത്തുകളുടെ ഒരു സ്ട്രിംഗ് പരിഗണിക്കുക; ഒരു പ്രോട്ടീൻ മടക്കുമ്പോൾ സംഭവിക്കുന്നത് ഇതാണ്. എന്നിരുന്നാലും, മുത്തുകളിൽ നിന്ന് വ്യത്യസ്തമായി, അമിനോ ആസിഡുകൾക്ക് തനതായ സ്വഭാവസവിശേഷതകൾ ഉണ്ട്, കൂടാതെ വിവിധ രീതികളിൽ പരസ്പരം ഇടപഴകുകയും പ്രോട്ടീൻ മടക്കിക്കളയുന്നത് സങ്കീർണ്ണവും സെൻസിറ്റീവായതുമായ ഒരു പ്രക്രിയയാക്കുന്നു.
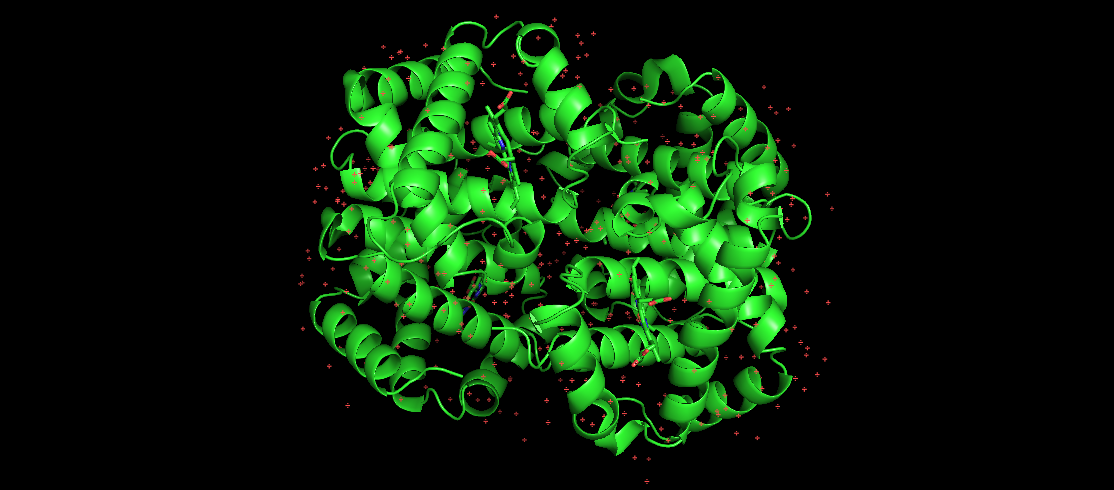
ഇവിടെയുള്ള ചിത്രം മനുഷ്യ ഹീമോഗ്ലോബിനെ പ്രതിനിധീകരിക്കുന്നു, ഇത് അറിയപ്പെടുന്ന ഒരു മടക്കിയ പ്രോട്ടീനാണ്
പ്രോട്ടീനുകൾ വേഗത്തിലും കൃത്യമായും മടക്കിക്കളയണം, അല്ലെങ്കിൽ അവ തെറ്റായി മടക്കി വികലമാകും. അത് അൽഷിമേഴ്സ്, പാർക്കിൻസൺസ് തുടങ്ങിയ രോഗങ്ങൾക്ക് കാരണമാകും. താപനില, മർദ്ദം, സെല്ലിലെ മറ്റ് തന്മാത്രകളുടെ സാന്നിധ്യം എന്നിവയെല്ലാം മടക്കുന്ന പ്രക്രിയയിൽ സ്വാധീനം ചെലുത്തുന്നു.
പതിറ്റാണ്ടുകൾ നീണ്ട ഗവേഷണത്തിനു ശേഷവും, പ്രോട്ടീനുകൾ എങ്ങനെ ചുരുങ്ങുന്നു എന്ന് കൃത്യമായി കണ്ടുപിടിക്കാൻ ശാസ്ത്രജ്ഞർ ഇപ്പോഴും ശ്രമിക്കുന്നു.
ഭാഗ്യവശാൽ, ആർട്ടിഫിഷ്യൽ ഇന്റലിജൻസിന്റെ പുരോഗതി ഈ മേഖലയിലെ വികസനം മെച്ചപ്പെടുത്തുന്നു. ഉപയോഗിച്ച് ശാസ്ത്രജ്ഞർക്ക് പ്രോട്ടീനുകളുടെ ഘടന മുമ്പത്തേക്കാളും കൃത്യമായി മുൻകൂട്ടി അറിയാൻ കഴിയും മെഷീൻ ലേണിംഗ് അൽഗോരിതംസ് ഡാറ്റയുടെ വലിയ അളവുകൾ പരിശോധിക്കാൻ.
മരുന്ന് വികസനം മാറ്റാനും രോഗത്തെക്കുറിച്ചുള്ള നമ്മുടെ തന്മാത്രാ അറിവ് വർദ്ധിപ്പിക്കാനും ഇതിന് കഴിവുണ്ട്.
യന്ത്രങ്ങൾക്ക് മികച്ച പ്രകടനം നടത്താൻ കഴിയുമോ?
പരമ്പരാഗത പ്രോട്ടീൻ ഫോൾഡിംഗ് ടെക്നിക്കുകൾക്ക് പരിമിതികളുണ്ട്
പതിറ്റാണ്ടുകളായി ശാസ്ത്രജ്ഞർ പ്രോട്ടീൻ ഫോൾഡിംഗ് കണ്ടുപിടിക്കാൻ ശ്രമിക്കുന്നു, എന്നാൽ പ്രക്രിയയുടെ സങ്കീർണ്ണത ഇതിനെ ഒരു വെല്ലുവിളി നിറഞ്ഞ വിഷയമാക്കി മാറ്റി.
പരമ്പരാഗത പ്രോട്ടീൻ ഘടന പ്രവചന സമീപനങ്ങൾ പരീക്ഷണാത്മക രീതികളുടെയും കമ്പ്യൂട്ടർ മോഡലിംഗിന്റെയും സംയോജനമാണ് ഉപയോഗിക്കുന്നത്, എന്നിരുന്നാലും, ഈ രീതികൾക്കെല്ലാം പോരായ്മകളുണ്ട്.
എക്സ്-റേ ക്രിസ്റ്റലോഗ്രാഫി, ന്യൂക്ലിയർ മാഗ്നെറ്റിക് റെസൊണൻസ് (എൻഎംആർ) തുടങ്ങിയ പരീക്ഷണാത്മക സാങ്കേതിക വിദ്യകൾ സമയമെടുക്കുന്നതും ചെലവേറിയതുമാണ്. കൂടാതെ, കമ്പ്യൂട്ടർ മോഡലുകൾ ചിലപ്പോൾ ലളിതമായ അനുമാനങ്ങളെ ആശ്രയിക്കുന്നു, അത് തെറ്റായ പ്രവചനങ്ങളിലേക്ക് നയിച്ചേക്കാം.
AI-ക്ക് ഈ തടസ്സങ്ങളെ മറികടക്കാൻ കഴിയും
ഭാഗ്യവശാൽ, നിർമ്മിത ബുദ്ധി കൂടുതൽ കൃത്യവും കാര്യക്ഷമവുമായ പ്രോട്ടീൻ ഘടന പ്രവചനത്തിന് പുതിയ വാഗ്ദാനം നൽകുന്നു. മെഷീൻ ലേണിംഗ് അൽഗോരിതങ്ങൾക്ക് വലിയ അളവിലുള്ള ഡാറ്റ പരിശോധിക്കാൻ കഴിയും. കൂടാതെ, ആളുകൾക്ക് നഷ്ടപ്പെടുന്ന പാറ്റേണുകൾ അവർ കണ്ടെത്തുന്നു.
പ്രോട്ടീൻ ഘടനയെ സമാനതകളില്ലാത്ത കൃത്യതയോടെ പ്രവചിക്കാൻ കഴിവുള്ള പുതിയ സോഫ്റ്റ്വെയർ ഉപകരണങ്ങളും പ്ലാറ്റ്ഫോമുകളും സൃഷ്ടിക്കുന്നതിന് ഇത് കാരണമായി.
പ്രോട്ടീൻ ഘടന പ്രവചനത്തിനായുള്ള ഏറ്റവും വാഗ്ദാനമായ മെഷീൻ ലേണിംഗ് അൽഗോരിതങ്ങൾ
ഗൂഗിൾ നിർമ്മിച്ച ആൽഫഫോൾഡ് സിസ്റ്റം ദീപ്പ് മൈൻഡ് ഈ മേഖലയിലെ ഏറ്റവും മികച്ച മുന്നേറ്റങ്ങളിലൊന്നാണ് ടീം. ഇത് ഉപയോഗിച്ചുകൊണ്ട് സമീപ വർഷങ്ങളിൽ വലിയ പുരോഗതി നേടിയിട്ടുണ്ട് ആഴത്തിലുള്ള പഠന അൽഗോരിതംസ് പ്രോട്ടീനുകളുടെ അമിനോ ആസിഡ് സീക്വൻസുകളെ അടിസ്ഥാനമാക്കി അവയുടെ ഘടന പ്രവചിക്കാൻ.
പ്രോട്ടീൻ ഘടന പ്രവചിക്കുന്നതിനുള്ള വാഗ്ദാനങ്ങൾ കാണിക്കുന്ന കൂടുതൽ മെഷീൻ ലേണിംഗ് രീതികളിൽ ന്യൂറൽ നെറ്റ്വർക്കുകൾ, സപ്പോർട്ട് വെക്റ്റർ മെഷീനുകൾ, ക്രമരഹിത വനങ്ങൾ എന്നിവ ഉൾപ്പെടുന്നു.
ഈ അൽഗോരിതങ്ങൾക്ക് വലിയ ഡാറ്റാസെറ്റുകളിൽ നിന്ന് പഠിക്കാൻ കഴിയും. കൂടാതെ, വ്യത്യസ്ത അമിനോ ആസിഡുകൾ തമ്മിലുള്ള പരസ്പരബന്ധം അവർക്ക് മുൻകൂട്ടി കാണാൻ കഴിയും. അതിനാൽ, ഇത് എങ്ങനെ പ്രവർത്തിക്കുന്നുവെന്ന് നോക്കാം.

സഹ-പരിണാമ വിശകലനങ്ങളും ആദ്യ ആൽഫഫോൾഡ് ജനറേഷനും
വിജയം ആൽഫഫോൾഡ് സഹ-പരിണാമ വിശകലനം ഉപയോഗിച്ച് വികസിപ്പിച്ചെടുത്ത ആഴത്തിലുള്ള ന്യൂറൽ നെറ്റ്വർക്ക് മോഡലിലാണ് നിർമ്മിച്ചിരിക്കുന്നത്. ഒരു പ്രോട്ടീനിലെ രണ്ട് അമിനോ ആസിഡുകൾ മറ്റൊന്നുമായി ഇടപഴകുകയാണെങ്കിൽ, അവയുടെ പ്രവർത്തനപരമായ ബന്ധം നിലനിർത്താൻ അവ ഒരുമിച്ച് വികസിക്കുമെന്ന് കോ-പരിണാമത്തിന്റെ ആശയം പറയുന്നു.
സമാനമായ നിരവധി പ്രോട്ടീനുകളുടെ അമിനോ ആസിഡ് സീക്വൻസുകൾ താരതമ്യം ചെയ്തുകൊണ്ട് 3D ഘടനയിൽ ഏതൊക്കെ ജോഡി അമിനോ ആസിഡുകളാണ് സമ്പർക്കം പുലർത്തുന്നതെന്ന് ഗവേഷകർക്ക് കണ്ടെത്താനാകും.
ആൽഫഫോൾഡിന്റെ ആദ്യ ആവർത്തനത്തിനുള്ള അടിത്തറയായി ഈ ഡാറ്റ പ്രവർത്തിക്കുന്നു. അമിനോ ആസിഡ് ജോഡികൾ തമ്മിലുള്ള നീളവും അവയെ ബന്ധിപ്പിക്കുന്ന പെപ്റ്റൈഡ് ബോണ്ടുകളുടെ കോണുകളും ഇത് പ്രവചിക്കുന്നു. വ്യക്തമായ ടെംപ്ലേറ്റുകളില്ലാത്ത പ്രോട്ടീനുകൾക്ക് ഇപ്പോഴും കൃത്യത പരിമിതപ്പെടുത്തിയിട്ടുണ്ടെങ്കിലും, ക്രമത്തിൽ നിന്ന് പ്രോട്ടീൻ ഘടന പ്രവചിക്കുന്നതിനുള്ള എല്ലാ മുൻ സമീപനങ്ങളെയും ഈ രീതി മറികടന്നു.

ആൽഫഫോൾഡ് 2: സമൂലമായി പുതിയ രീതിശാസ്ത്രം
പ്രോട്ടീന്റെ 2D ഘടന പ്രവചിക്കാൻ പ്രോട്ടീന്റെ അമിനോ ആസിഡ് സീക്വൻസ് ഉപയോഗിക്കുന്ന DeepMind സൃഷ്ടിച്ച ഒരു കമ്പ്യൂട്ടർ സോഫ്റ്റ്വെയറാണ് AlphaFold3.
ഒരു പ്രോട്ടീന്റെ ഘടന അത് എങ്ങനെ പ്രവർത്തിക്കുന്നുവെന്ന് നിർണ്ണയിക്കുന്നതിനാൽ ഇത് വളരെ പ്രധാനമാണ്, കൂടാതെ അതിന്റെ പ്രവർത്തനം മനസ്സിലാക്കുന്നത് പ്രോട്ടീനിനെ ലക്ഷ്യം വയ്ക്കുന്ന മരുന്നുകൾ വികസിപ്പിക്കാൻ ശാസ്ത്രജ്ഞരെ സഹായിക്കും.
ആൽഫഫോൾഡ്2 ന്യൂറൽ നെറ്റ്വർക്ക് പ്രോട്ടീന്റെ അമിനോ ആസിഡ് സീക്വൻസും ഒരു ഡാറ്റാബേസിലെ മറ്റ് സീക്വൻസുകളുമായി എങ്ങനെ താരതമ്യം ചെയ്യുന്നു എന്നതിനെക്കുറിച്ചുള്ള വിശദാംശങ്ങളും ഇൻപുട്ടായി സ്വീകരിക്കുന്നു (ഇതിനെ "സീക്വൻസ് അലൈൻമെന്റ്" എന്ന് വിളിക്കുന്നു).
ഈ ഇൻപുട്ടിനെ അടിസ്ഥാനമാക്കി പ്രോട്ടീന്റെ 3D ഘടനയെക്കുറിച്ച് ന്യൂറൽ നെറ്റ്വർക്ക് ഒരു പ്രവചനം നടത്തുന്നു.
ആൽഫഫോൾഡ് 2 ൽ നിന്ന് ഇതിനെ വേർതിരിക്കുന്നത് എന്താണ്?
മറ്റ് സമീപനങ്ങളിൽ നിന്ന് വ്യത്യസ്തമായി, ആൽഫഫോൾഡ്2 പ്രോട്ടീന്റെ യഥാർത്ഥ 3D ഘടനയെ പ്രവചിക്കുന്നു, അമിനോ ആസിഡുകളുടെ ജോഡികൾ തമ്മിലുള്ള വേർപിരിയൽ അല്ലെങ്കിൽ അവയെ ബന്ധിപ്പിക്കുന്ന ബോണ്ടുകൾ തമ്മിലുള്ള കോണുകൾ (മുൻ അൽഗോരിതം ചെയ്തതുപോലെ).
ന്യൂറൽ നെറ്റ്വർക്കിന് മുഴുവൻ ഘടനയും ഒരേസമയം മുൻകൂട്ടി അറിയുന്നതിന്, ഘടന എൻഡ്-ടു-എൻഡ് എൻകോഡ് ചെയ്യുന്നു.
AlphaFold2-ന്റെ മറ്റൊരു പ്രധാന സ്വഭാവം, അത് അതിന്റെ പ്രവചനത്തിൽ എത്രത്തോളം ആത്മവിശ്വാസം പുലർത്തുന്നു എന്നതിന്റെ ഒരു കണക്ക് നൽകുന്നു എന്നതാണ്. ഇത് പ്രതീക്ഷിക്കുന്ന ഘടനയിൽ ഒരു കളർ കോഡിംഗായി അവതരിപ്പിക്കുന്നു, ചുവപ്പ് ഉയർന്ന ആത്മവിശ്വാസത്തെയും നീല കുറഞ്ഞ ആത്മവിശ്വാസത്തെയും പ്രതിനിധീകരിക്കുന്നു.
പ്രവചനത്തിന്റെ സ്ഥിരതയെക്കുറിച്ച് ശാസ്ത്രജ്ഞരെ അറിയിക്കുന്നതിനാൽ ഇത് ഉപയോഗപ്രദമാണ്.
നിരവധി സീക്വൻസുകളുടെ സംയോജിത ഘടന പ്രവചിക്കുന്നു
ആൽഫഫോൾഡ് മൾട്ടിമർ എന്നറിയപ്പെടുന്ന ആൽഫഫോൾഡ്2 ന്റെ ഏറ്റവും പുതിയ വിപുലീകരണം, നിരവധി സീക്വൻസുകളുടെ സംയോജിത ഘടന പ്രവചിക്കുന്നു. മുമ്പത്തെ സാങ്കേതികതകളേക്കാൾ മികച്ച പ്രകടനം കാഴ്ചവെച്ചാലും ഇതിന് ഇപ്പോഴും ഉയർന്ന പിഴവ് നിരക്കുകൾ ഉണ്ട്. 25 പ്രോട്ടീൻ കോംപ്ലക്സുകളിൽ 4500% മാത്രമേ വിജയകരമായി പ്രവചിക്കപ്പെട്ടിട്ടുള്ളൂ.
കോൺടാക്റ്റ് രൂപീകരണത്തിന്റെ പരുക്കൻ പ്രദേശങ്ങളിൽ 70% ശരിയായി പ്രവചിക്കപ്പെട്ടിരുന്നു, എന്നാൽ രണ്ട് പ്രോട്ടീനുകളുടെ ആപേക്ഷിക ഓറിയന്റേഷൻ തെറ്റായിരുന്നു. മീഡിയൻ അലൈൻമെന്റ് ഡെപ്ത് ഏകദേശം 30 സീക്വൻസുകളിൽ കുറവായിരിക്കുമ്പോൾ, ആൽഫഫോൾഡ് മൾട്ടിമർ പ്രവചനങ്ങളുടെ കൃത്യത ഗണ്യമായി കുറയുന്നു.
ആൽഫഫോൾഡ് പ്രവചനങ്ങൾ എങ്ങനെ ഉപയോഗിക്കാം
ആൽഫഫോൾഡിൽ നിന്നുള്ള പ്രവചിച്ച മോഡലുകൾ ഒരേ ഫയൽ ഫോർമാറ്റിലാണ് വാഗ്ദാനം ചെയ്യുന്നത് കൂടാതെ പരീക്ഷണാത്മക ഘടനകൾ പോലെ തന്നെ ഉപയോഗിക്കാനും കഴിയും. തെറ്റിദ്ധാരണകൾ തടയുന്നതിന് മോഡലിനൊപ്പം നൽകിയിരിക്കുന്ന കൃത്യത കണക്കുകൾ കണക്കിലെടുക്കേണ്ടത് പ്രധാനമാണ്.
ഇഴചേർന്ന ഹോമോമറുകൾ അല്ലെങ്കിൽ പ്രോട്ടീനുകൾ പോലുള്ള സങ്കീർണ്ണമായ ഘടനകൾക്ക് ഇത് പ്രത്യേകിച്ചും സഹായകരമാണ്.
അജ്ഞാത ലിഗാൻഡ്.
ചില വെല്ലുവിളികൾ
പ്രോട്ടീനിലേക്കും ബയോഫിസിക്കൽ ഡാറ്റയിലേക്കും പ്രവേശനമില്ലാതെ ബൈൻഡിംഗിന്റെ ചലനാത്മകത, ലിഗാൻഡ് സെലക്റ്റിവിറ്റി, നിയന്ത്രണം, അലോസ്റ്ററി, പോസ്റ്റ്-ട്രാൻസ്ലേഷണൽ മാറ്റങ്ങൾ, ചലനാത്മകത എന്നിവ മനസ്സിലാക്കുന്നതാണ് പ്രവചിക്കപ്പെട്ട ഘടനകൾ ഉപയോഗിക്കുന്നതിലെ പ്രധാന പ്രശ്നം.
യന്ത്ര പഠനം ഈ പ്രശ്നം മറികടക്കാൻ ഭൗതികശാസ്ത്രത്തെ അടിസ്ഥാനമാക്കിയുള്ള മോളിക്യുലാർ ഡൈനാമിക്സ് ഗവേഷണം ഉപയോഗപ്പെടുത്താം.
ഈ അന്വേഷണങ്ങൾ വിദഗ്ദ്ധവും കാര്യക്ഷമവുമായ കമ്പ്യൂട്ടർ ആർക്കിടെക്ചറിൽ നിന്ന് പ്രയോജനം നേടിയേക്കാം. പ്രോട്ടീൻ ഘടനകൾ പ്രവചിക്കുന്നതിൽ ആൽഫഫോൾഡ് വമ്പിച്ച മുന്നേറ്റം കൈവരിച്ചിട്ടുണ്ടെങ്കിലും, ഘടനാപരമായ ജീവശാസ്ത്ര മേഖലയിൽ ഇനിയും ഏറെ പഠിക്കാനുണ്ട്, ആൽഫഫോൾഡ് പ്രവചനങ്ങൾ ഭാവിയിലെ പഠനത്തിന്റെ ആരംഭ പോയിന്റ് മാത്രമാണ്.
മറ്റ് ശ്രദ്ധേയമായ ഉപകരണങ്ങൾ എന്തൊക്കെയാണ്?
RoseTTAFold
വാഷിംഗ്ടൺ സർവകലാശാലയിലെ ഗവേഷകർ സൃഷ്ടിച്ച RoseTTAFold, പ്രോട്ടീൻ ഘടനകളെ പ്രവചിക്കാൻ ആഴത്തിലുള്ള പഠന അൽഗോരിതങ്ങൾ ഉപയോഗിക്കുന്നു, എന്നാൽ പ്രവചിക്കപ്പെട്ട ഘടനകൾ മെച്ചപ്പെടുത്തുന്നതിന് "ടോർഷൻ ആംഗിൾ ഡൈനാമിക്സ് സിമുലേഷൻസ്" എന്നറിയപ്പെടുന്ന ഒരു നവീന സമീപനവും ഇത് സമന്വയിപ്പിക്കുന്നു.
ഈ രീതി പ്രോത്സാഹജനകമായ ഫലങ്ങൾ നൽകി, നിലവിലുള്ള AI പ്രോട്ടീൻ ഫോൾഡിംഗ് ടൂളുകളുടെ പരിമിതികൾ മറികടക്കാൻ ഇത് ഉപയോഗപ്രദമാകും.
ട്രോസെറ്റ
മറ്റൊരു ഉപകരണം, ട്രോസെറ്റ, ഒരു ഉപയോഗിച്ച് പ്രോട്ടീൻ മടക്കിക്കളയുന്നത് പ്രവചിക്കുന്നു ന്യൂറൽ നെറ്റ്വർക്ക് ദശലക്ഷക്കണക്കിന് പ്രോട്ടീൻ സീക്വൻസുകളിലും ഘടനകളിലും പരിശീലനം നേടി.
ടാർഗെറ്റ് പ്രോട്ടീനിനെ താരതമ്യപ്പെടുത്താവുന്ന അറിയപ്പെടുന്ന ഘടനകളുമായി താരതമ്യം ചെയ്തുകൊണ്ട് കൂടുതൽ കൃത്യമായ പ്രവചനങ്ങൾ സൃഷ്ടിക്കുന്നതിന് ഇത് ഒരു "ടെംപ്ലേറ്റ് അടിസ്ഥാനമാക്കിയുള്ള മോഡലിംഗ്" സാങ്കേതികത ഉപയോഗിക്കുന്നു.
ചെറിയ പ്രോട്ടീനുകളുടെയും പ്രോട്ടീൻ കോംപ്ലക്സുകളുടെയും ഘടന പ്രവചിക്കാൻ ട്രോസെറ്റയ്ക്ക് കഴിയുമെന്ന് തെളിയിക്കപ്പെട്ടിട്ടുണ്ട്.
DeepMetaPSICOV
പ്രോട്ടീൻ കോൺടാക്റ്റ് മാപ്പുകൾ പ്രവചിക്കുന്നതിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കുന്ന മറ്റൊരു ഉപകരണമാണ് DeepMetaPSICOV. പ്രോട്ടീൻ മടക്കുകൾ പ്രവചിക്കുന്നതിനുള്ള ഒരു ഗൈഡായി ഇവ ഉപയോഗിക്കുന്നു. അത് ഉപയോഗിക്കുന്നു ആഴത്തിലുള്ള പഠനം പ്രോട്ടീനിനുള്ളിലെ അവശിഷ്ട പ്രതിപ്രവർത്തനങ്ങളുടെ സാധ്യത പ്രവചിക്കാനുള്ള സമീപനങ്ങൾ.
മൊത്തത്തിലുള്ള കോൺടാക്റ്റ് മാപ്പ് പ്രവചിക്കാൻ ഇവ പിന്നീട് ഉപയോഗിക്കുന്നു. മുൻ സമീപനങ്ങൾ പരാജയപ്പെട്ടപ്പോൾ പോലും, വളരെ കൃത്യതയോടെ പ്രോട്ടീൻ ഘടനകളെ പ്രവചിക്കുന്നതിൽ DeepMetaPSICOV കഴിവ് തെളിയിച്ചിട്ടുണ്ട്.
ഭാവി എന്തായിരിക്കും?
AI പ്രോട്ടീൻ ഫോൾഡിംഗിന്റെ ഭാവി ശോഭനമാണ്. പ്രോട്ടീൻ ഘടനകളെ വിശ്വസനീയമായി പ്രവചിക്കുന്നതിൽ ആഴത്തിലുള്ള പഠന-അധിഷ്ഠിത അൽഗോരിതങ്ങൾ, പ്രത്യേകിച്ച് ആൽഫഫോൾഡ്2, അടുത്തിടെ വലിയ പുരോഗതി കൈവരിച്ചിട്ടുണ്ട്.
സാധാരണ ചികിത്സാ ലക്ഷ്യങ്ങളായ പ്രോട്ടീനുകളുടെ ഘടനയും പ്രവർത്തനവും നന്നായി മനസ്സിലാക്കാൻ ശാസ്ത്രജ്ഞരെ അനുവദിച്ചുകൊണ്ട് ഈ കണ്ടെത്തലിന് മയക്കുമരുന്ന് വികസനം മാറ്റാനുള്ള കഴിവുണ്ട്.
എന്നിരുന്നാലും, പ്രോട്ടീൻ കോംപ്ലക്സുകൾ പ്രവചിക്കുക, പ്രതീക്ഷിക്കുന്ന ഘടനകളുടെ യഥാർത്ഥ പ്രവർത്തന നില കണ്ടെത്തുക തുടങ്ങിയ പ്രശ്നങ്ങൾ അവശേഷിക്കുന്നു. ഈ പ്രശ്നങ്ങൾ പരിഹരിക്കുന്നതിനും AI പ്രോട്ടീൻ ഫോൾഡിംഗ് അൽഗോരിതങ്ങളുടെ കൃത്യതയും വിശ്വാസ്യതയും വർദ്ധിപ്പിക്കുന്നതിനും കൂടുതൽ ഗവേഷണം ആവശ്യമാണ്.
എന്നിരുന്നാലും, ഈ സാങ്കേതികവിദ്യയുടെ സാധ്യതയുള്ള നേട്ടങ്ങൾ വളരെ വലുതാണ്, കൂടുതൽ ഫലപ്രദവും കൃത്യവുമായ മരുന്നുകളുടെ ഉൽപാദനത്തിലേക്ക് നയിക്കാനുള്ള കഴിവുണ്ട്.





നിങ്ങളുടെ അഭിപ്രായങ്ങൾ രേഖപ്പെടുത്തുക