Ko darīt, ja mēs varētu izmantot mākslīgo intelektu, lai atbildētu uz vienu no dzīves lielākajiem noslēpumiem – olbaltumvielu locīšanu? Zinātnieki pie tā ir strādājuši gadu desmitiem.
Mašīnas tagad var paredzēt olbaltumvielu struktūras ar pārsteidzošu precizitāti, izmantojot dziļās mācīšanās modeļus, mainot zāļu izstrādi, biotehnoloģiju un mūsu zināšanas par fundamentālajiem bioloģiskajiem procesiem.
Pievienojieties man, lai izpētītu intriģējošo mākslīgā intelekta proteīnu locīšanas jomu, kur jaunākās tehnoloģijas saduras ar pašas dzīves sarežģītību.
Olbaltumvielu locīšanas noslēpuma atšķetināšana
Olbaltumvielas mūsu ķermeņos darbojas kā mazas mašīnas, lai veiktu tādus svarīgus uzdevumus kā pārtikas sadalīšana vai skābekļa transportēšana. Tām jābūt pareizi salocītām, lai tās darbotos efektīvi, tāpat kā atslēgai ir pareizi jāsagriež, lai tās ietilptu slēdzenē. Tiklīdz proteīns ir izveidots, sākas ļoti sarežģīts locīšanas process.
Olbaltumvielu locīšana ir process, kurā garas aminoskābju ķēdes, proteīna celtniecības bloki, salokās trīsdimensiju struktūrās, kas nosaka proteīna funkciju.
Apsveriet garu krelles virkni, kas jāsakārto precīzā formā; tas notiek, kad proteīns salocās. Tomēr atšķirībā no krellēm aminoskābēm ir unikālas īpašības un tās dažādos veidos mijiedarbojas, padarot olbaltumvielu locīšanu par sarežģītu un jutīgu procesu.
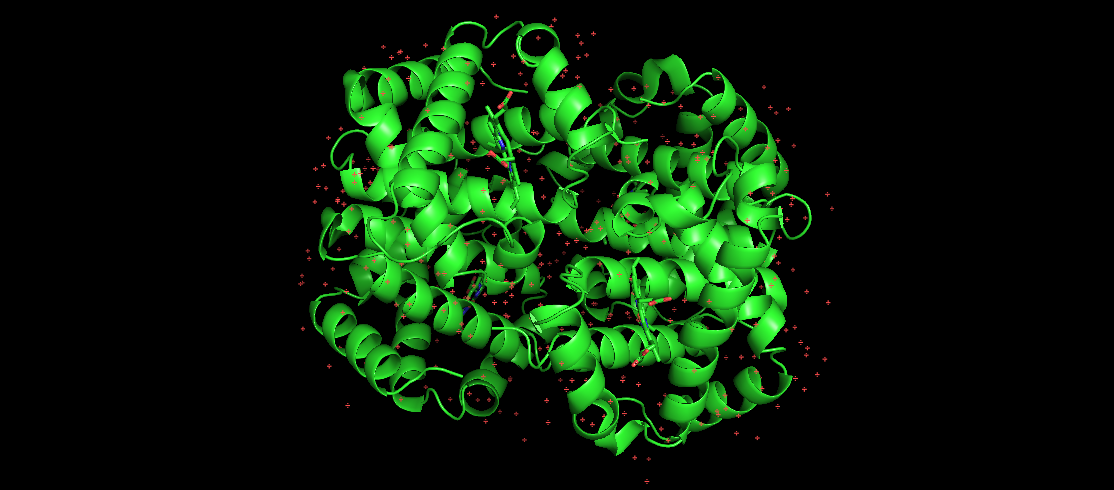
Attēlā redzams cilvēka hemoglobīns, kas ir labi zināms salocīts proteīns
Proteīniem ir jāsaloka ātri un precīzi, pretējā gadījumā tie kļūs nepareizi salocīti un bojāti. Tas var izraisīt tādas slimības kā Alcheimera un Parkinsona slimība. Temperatūra, spiediens un citu molekulu klātbūtne šūnā ietekmē locīšanas procesu.
Pēc gadu desmitiem ilgiem pētījumiem zinātnieki joprojām cenšas precīzi noskaidrot, kā proteīni salokās.
Par laimi mākslīgā intelekta sasniegumi uzlabo nozares attīstību. Zinātnieki var precīzāk nekā jebkad agrāk paredzēt olbaltumvielu struktūru, izmantojot mašīnmācīšanās algoritmi lai pārbaudītu milzīgus datu apjomus.
Tas var mainīt zāļu izstrādi un palielināt mūsu molekulārās zināšanas par slimību.
Vai mašīnas var darboties labāk?
Parastajām olbaltumvielu locīšanas metodēm ir ierobežojumi
Zinātnieki gadu desmitiem ir mēģinājuši izdomāt olbaltumvielu locīšanu, taču procesa sarežģītība ir padarījusi šo tēmu par sarežģītu.
Tradicionālās proteīna struktūras prognozēšanas pieejas izmanto eksperimentālo metodoloģiju un datormodelēšanas kombināciju, tomēr visām šīm metodēm ir trūkumi.
Eksperimentālās metodes, piemēram, rentgenstaru kristalogrāfija un kodolmagnētiskā rezonanse (KMR), var būt laikietilpīgas un dārgas. Un datormodeļi dažkārt paļaujas uz vienkāršiem pieņēmumiem, kas var izraisīt kļūdainas prognozes.
AI var pārvarēt šos šķēršļus
Par laimi, mākslīgais intelekts sniedz jaunu solījumu precīzākai un efektīvākai olbaltumvielu struktūras prognozēšanai. Mašīnmācīšanās algoritmi var pārbaudīt milzīgus datu apjomus. Un viņi atklāj modeļus, kurus cilvēki palaistu garām.
Tā rezultātā ir izveidoti jauni programmatūras rīki un platformas, kas spēj paredzēt olbaltumvielu struktūru ar nepārspējamu precizitāti.
Daudzsološākie mašīnmācīšanās algoritmi proteīna struktūras prognozēšanai
AlphaFold sistēma, ko izveidojis Google Deepmind komanda ir viens no daudzsološākajiem sasniegumiem šajā jomā. Pēdējos gados tas ir guvis lielu progresu, izmantojot dziļi mācīšanās algoritmi prognozēt proteīnu struktūru, pamatojoties uz to aminoskābju sekvencēm.
Neironu tīkli, atbalsta vektoru mašīnas un nejauši meži ir vienas no vairākām mašīnmācīšanās metodēm, kas liecina par solījumu prognozēt olbaltumvielu struktūru.
Šie algoritmi var mācīties no milzīgām datu kopām. Un viņi var paredzēt korelācijas starp dažādām aminoskābēm. Tātad, redzēsim, kā tas darbojas.

Kopīgās evolūcijas analīzes un pirmā AlphaFold paaudze
Panākumi AlphaFold ir veidots uz dziļa neironu tīkla modeļa, kas tika izstrādāts, izmantojot koevolūcijas analīzi. Koevolūcijas koncepcija nosaka, ka, ja divas proteīna aminoskābes mijiedarbojas viena ar otru, tās attīstīsies kopā, lai saglabātu savu funkcionālo saikni.
Pētnieki var noteikt, kuri aminoskābju pāri, iespējams, ir saskarē 3D struktūrā, salīdzinot daudzu līdzīgu proteīnu aminoskābju secības.
Šie dati kalpo par pamatu pirmajai AlphaFold iterācijai. Tas paredz garumus starp aminoskābju pāriem, kā arī peptīdu saišu leņķus, kas tos savieno. Šī metode pārspēja visas iepriekšējās pieejas proteīna struktūras prognozēšanai no secības, lai gan precizitāte joprojām bija ierobežota proteīniem bez redzamām veidnēm.

AlphaFold 2: radikāli jauna metodika
AlphaFold2 ir DeepMind izveidota datora programmatūra, kas izmanto proteīna aminoskābju secību, lai prognozētu proteīna 3D struktūru.
Tas ir svarīgi, jo proteīna struktūra nosaka, kā tā darbojas, un izpratne par tās funkciju var palīdzēt zinātniekiem izstrādāt zāles, kuru mērķis ir proteīns.
AlphaFold2 neironu tīkls kā ievadi saņem proteīna aminoskābju secību, kā arī sīkāku informāciju par to, kā šī secība tiek salīdzināta ar citām datubāzes sekvencēm (to sauc par "secības saskaņošanu").
Neironu tīkls, pamatojoties uz šo ievadi, prognozē proteīna 3D struktūru.
Kas to atšķir no AlphaFold2?
Atšķirībā no citām pieejām AlphaFold2 prognozē proteīna reālo 3D struktūru, nevis tikai atdalīšanu starp aminoskābju pāriem vai leņķus starp saitēm, kas tos savieno (kā to darīja iepriekšējie algoritmi).
Lai neironu tīkls varētu paredzēt visu struktūru uzreiz, struktūra tiek kodēta no gala līdz galam.
Vēl viena svarīga AlphaFold2 īpašība ir tā, ka tā piedāvā aplēses par to, cik pārliecināts tas ir par savu prognozi. Tas tiek attēlots kā paredzamās struktūras krāsu kods, ar sarkanu apzīmē augstu ticamību un zilu norāda uz zemu ticamību.
Tas ir noderīgi, jo informē zinātniekus par prognozes stabilitāti.
Vairāku secību kombinētās struktūras prognozēšana
Jaunākais Alphafold2 paplašinājums, kas pazīstams kā Alphafold Multimer, prognozē vairāku secību apvienoto struktūru. Tam joprojām ir augsts kļūdu līmenis, pat ja tas darbojas daudz labāk nekā iepriekšējās metodes. Tikai % 25 no 4500 proteīnu kompleksiem tika veiksmīgi prognozēti.
70% kontaktu veidošanās aptuveno reģionu tika pareizi prognozēti, bet abu proteīnu relatīvā orientācija bija nepareiza. Ja vidējais izlīdzināšanas dziļums ir mazāks par aptuveni 30 sekvencēm, Alphafold multimēra prognožu precizitāte ievērojami samazinās.
Kā izmantot alfafolda prognozes
AlphaFold prognozētie modeļi tiek piedāvāti tajos pašos failu formātos, un tos var izmantot tāpat kā eksperimentālās struktūras. Ir ļoti svarīgi ņemt vērā modelī piedāvātos precizitātes aprēķinus, lai novērstu pārpratumus.
Tas ir īpaši noderīgi sarežģītām struktūrām, piemēram, savstarpēji saistītiem homomēriem vai proteīniem, kas salokās tikai
nezināms ligands.
Daži izaicinājumi
Galvenā problēma paredzēto struktūru izmantošanā ir izpratne par dinamiku, ligandu selektivitāti, kontroli, allostēriju, pēctranslācijas izmaiņām un saistīšanās kinētiku bez piekļuves olbaltumvielām un biofizikālajiem datiem.
mašīna mācīšanās un, lai pārvarētu šo problēmu, var izmantot uz fiziku balstītus molekulārās dinamikas pētījumus.
Šie pētījumi var gūt labumu no specializētas un efektīvas datoru arhitektūras. Lai gan AlphaFold ir sasniegusi milzīgus panākumus olbaltumvielu struktūru prognozēšanā, strukturālās bioloģijas jomā joprojām ir daudz ko mācīties, un AlphaFold prognozes ir tikai sākumpunkts turpmākajiem pētījumiem.
Kādi ir citi ievērojami rīki?
RoseTTAFold
RoseTTAFold, ko izveidojuši Vašingtonas Universitātes pētnieki, arī izmanto dziļas mācīšanās algoritmus, lai prognozētu olbaltumvielu struktūras, taču tajā ir arī integrēta jauna pieeja, kas pazīstama kā "vērpes leņķa dinamikas simulācijas", lai uzlabotu prognozētās struktūras.
Šī metode ir devusi iepriecinošus rezultātus un var būt noderīga, lai pārvarētu esošo AI proteīna locīšanas rīku ierobežojumus.
trRosetta
Vēl viens rīks, trRosetta, prognozē olbaltumvielu locīšanu, izmantojot a neironu tīklu apmācīts miljoniem olbaltumvielu sekvenču un struktūru.
Tas izmanto arī uz veidni balstītu modelēšanas paņēmienu, lai radītu precīzākas prognozes, salīdzinot mērķa proteīnu ar salīdzināmām zināmām struktūrām.
Ir pierādīts, ka trRosetta spēj paredzēt sīku proteīnu un proteīnu kompleksu struktūras.
DeepMetaPSICOV
DeepMetaPSICOV ir vēl viens rīks, kas koncentrējas uz olbaltumvielu kontaktu karšu prognozēšanu. Tie tiek izmantoti kā ceļvedis, lai prognozētu olbaltumvielu locīšanu. Tā izmanto dziļa mācīšanās pieejas, lai prognozētu atlieku mijiedarbības iespējamību proteīnā.
Pēc tam tos izmanto, lai prognozētu kopējo kontaktu karti. DeepMetaPSICOV ir parādījis potenciālu proteīnu struktūru prognozēšanā ar lielu precizitāti, pat ja iepriekšējās pieejas ir bijušas neveiksmīgas.
Ko tur nākotne?
AI proteīna locīšanas nākotne ir gaiša. Uz dziļu mācīšanos balstīti algoritmi, jo īpaši AlphaFold2, nesen ir guvuši lielu progresu proteīnu struktūru ticamā prognozēšanā.
Šis atklājums var pārveidot zāļu izstrādi, ļaujot zinātniekiem labāk izprast proteīnu struktūru un funkcijas, kas ir izplatīti terapeitiskie mērķi.
Tomēr joprojām pastāv tādi jautājumi kā proteīnu kompleksu prognozēšana un paredzamo struktūru reālā funkcionālā stāvokļa noteikšana. Ir nepieciešams vairāk pētījumu, lai atrisinātu šīs problēmas un palielinātu AI proteīna locīšanas algoritmu precizitāti un uzticamību.
Tomēr šīs tehnoloģijas potenciālie ieguvumi ir milzīgi, un tas var novest pie efektīvāku un precīzāku medikamentu ražošanas.





Atstāj atbildi