کیا ہوگا اگر ہم مصنوعی ذہانت کو زندگی کے سب سے بڑے اسرار یعنی پروٹین فولڈنگ کا جواب دینے کے لیے استعمال کر سکیں؟ سائنسدان کئی دہائیوں سے اس پر کام کر رہے ہیں۔
مشینیں اب گہرے سیکھنے کے ماڈلز، منشیات کی نشوونما، بائیو ٹیکنالوجی، اور بنیادی حیاتیاتی عمل کے بارے میں ہمارے علم کو تبدیل کرتے ہوئے حیرت انگیز درستگی کے ساتھ پروٹین کے ڈھانچے کی پیش گوئی کر سکتی ہیں۔
AI پروٹین فولڈنگ کے دلچسپ دائرے کی تلاش میں میرے ساتھ شامل ہوں، جہاں جدید ٹیکنالوجی خود زندگی کی پیچیدگی سے ٹکرا جاتی ہے۔
پروٹین فولڈنگ کے اسرار کو کھولنا
پروٹین ہمارے جسموں میں چھوٹی مشینوں کی طرح کام کرتے ہیں جیسے کھانے کو توڑنا یا آکسیجن پہنچانا۔ ان کے مؤثر طریقے سے کام کرنے کے لیے انہیں صحیح طریقے سے فولڈ کیا جانا چاہیے، بالکل اسی طرح جیسے تالے میں فٹ ہونے کے لیے چابی کو درست طریقے سے کاٹا جانا چاہیے۔ جیسے ہی پروٹین بنتا ہے، فولڈنگ کا ایک بہت ہی پیچیدہ عمل شروع ہو جاتا ہے۔
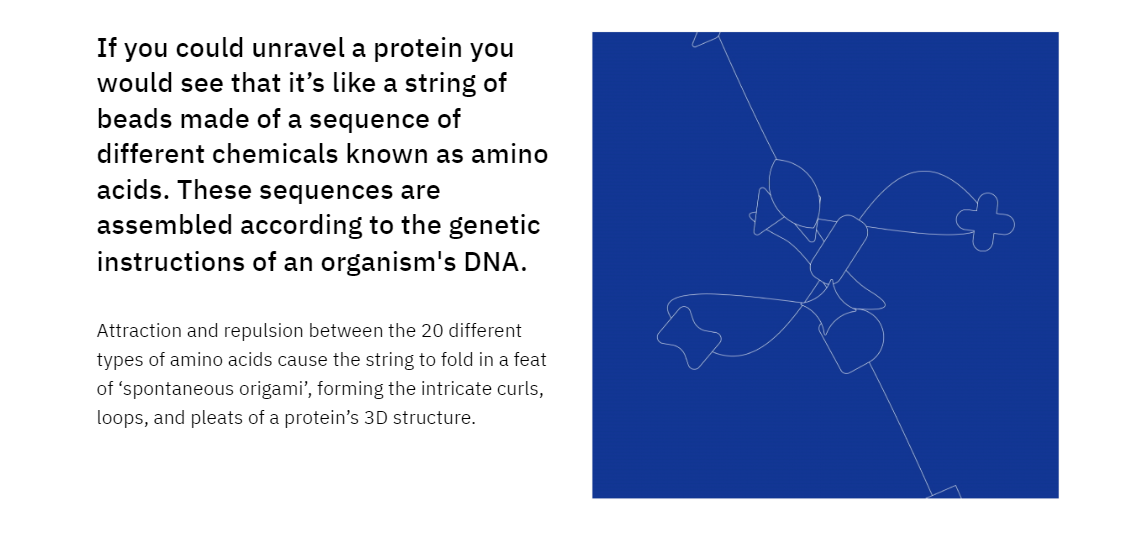
پروٹین فولڈنگ ایک ایسا عمل ہے جس کے ذریعے امینو ایسڈ کی لمبی زنجیریں، پروٹین کے بلڈنگ بلاکس، تین جہتی ڈھانچے میں جوڑتے ہیں جو پروٹین کے کام کا حکم دیتے ہیں۔
موتیوں کی ایک لمبی تار پر غور کریں جو ایک عین شکل میں ترتیب دینا ضروری ہے؛ یہ وہی ہوتا ہے جب ایک پروٹین فولڈ ہوتا ہے۔ پھر بھی، موتیوں کے برعکس، امینو ایسڈ منفرد خصوصیات کے حامل ہوتے ہیں اور مختلف طریقوں سے ایک دوسرے کے ساتھ تعامل کرتے ہیں، جس سے پروٹین فولڈنگ کو ایک پیچیدہ اور حساس عمل بناتا ہے۔
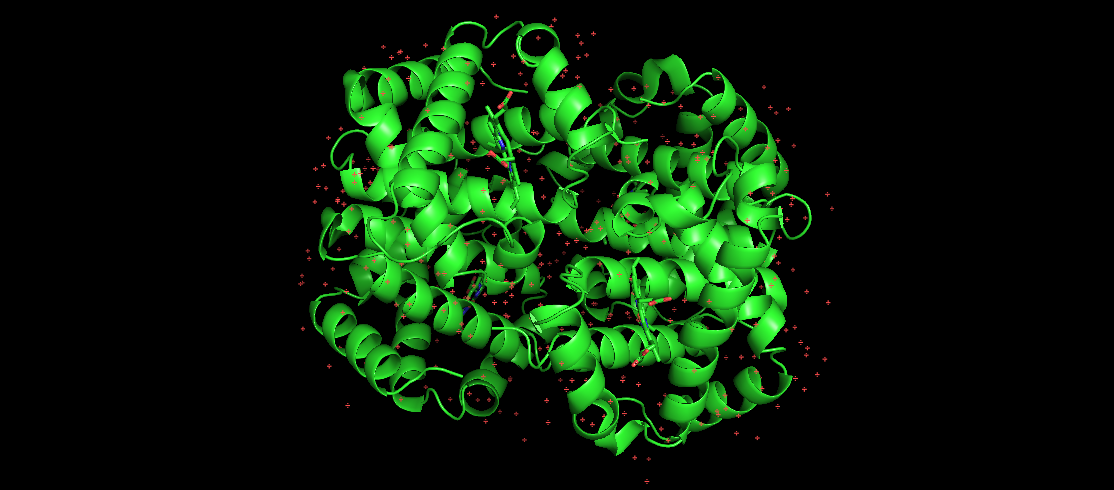
یہاں کی تصویر انسانی ہیموگلوبن کی نمائندگی کرتی ہے، جو کہ ایک معروف فولڈ پروٹین ہے۔
پروٹین کو تیزی سے اور درست طریقے سے فولڈ ہونا چاہیے، ورنہ وہ غلط فولڈ اور خراب ہو جائیں گے۔ یہ الزائمر اور پارکنسنز جیسی بیماریوں کا باعث بن سکتا ہے۔ درجہ حرارت، دباؤ، اور خلیے میں دوسرے مالیکیولز کی موجودگی کا اثر فولڈنگ کے عمل پر پڑتا ہے۔
کئی دہائیوں کی تحقیق کے بعد، سائنسدان ابھی تک یہ جاننے کی کوشش کر رہے ہیں کہ پروٹین کیسے فولڈ ہوتے ہیں۔
شکر ہے، مصنوعی ذہانت میں پیش رفت اس شعبے میں ترقی کو بہتر بنا رہی ہے۔ سائنسدان پروٹین کی ساخت کا پہلے سے کہیں زیادہ درست طریقے سے استعمال کر کے اندازہ لگا سکتے ہیں۔ مشین لرننگ الگورتھم ڈیٹا کے بڑے حجم کا جائزہ لینے کے لیے۔
اس میں دواؤں کی نشوونما کو تبدیل کرنے اور بیماری کے بارے میں ہمارے مالیکیولر علم میں اضافہ کرنے کی صلاحیت ہے۔
کیا مشینیں بہتر کارکردگی کا مظاہرہ کر سکتی ہیں؟
روایتی پروٹین فولڈنگ تکنیک کی حدود ہیں۔
سائنسدان کئی دہائیوں سے پروٹین فولڈنگ کا پتہ لگانے کی کوشش کر رہے ہیں، لیکن اس عمل کی پیچیدگی نے اسے ایک چیلنجنگ موضوع بنا دیا ہے۔
روایتی پروٹین کی ساخت کی پیشن گوئی کے نقطہ نظر تجرباتی طریقوں اور کمپیوٹر ماڈلنگ کا ایک مجموعہ استعمال کرتے ہیں، تاہم، ان تمام طریقوں میں خامیاں ہیں۔
ایکس رے کرسٹالوگرافی اور نیوکلیئر میگنیٹک ریزوننس (NMR) جیسی تجرباتی تکنیکیں وقت طلب اور مہنگی ہو سکتی ہیں۔ اور، کمپیوٹر ماڈل بعض اوقات سادہ مفروضوں پر انحصار کرتے ہیں، جو غلط پیشین گوئیوں کا باعث بن سکتے ہیں۔
AI ان رکاوٹوں کو دور کر سکتا ہے۔
خوش قسمتی سے، مصنوعی ذہانت زیادہ درست اور موثر پروٹین کی ساخت کی پیشن گوئی کے لیے تازہ وعدہ فراہم کر رہا ہے۔ مشین لرننگ الگورتھم بڑے پیمانے پر ڈیٹا کی جانچ کر سکتے ہیں۔ اور، وہ ایسے نمونوں کو ننگا کرتے ہیں جن سے لوگ یاد کرتے ہیں۔
اس کے نتیجے میں نئے سافٹ ویئر ٹولز اور پلیٹ فارمز کی تخلیق ہوئی ہے جو بے مثال درستگی کے ساتھ پروٹین کی ساخت کی پیش گوئی کرنے کے قابل ہیں۔
پروٹین کی ساخت کی پیشن گوئی کے لیے سب سے زیادہ امید افزا مشین لرننگ الگورتھم
گوگل کے ذریعہ بنایا گیا الفا فولڈ سسٹم Deepmind ٹیم اس علاقے میں سب سے زیادہ امید افزا پیشرفت میں سے ایک ہے۔ اس کا استعمال کرتے ہوئے حالیہ برسوں میں بہت ترقی حاصل کی ہے گہری سیکھنے الگورتھم امینو ایسڈ کی ترتیب کی بنیاد پر پروٹین کی ساخت کی پیش گوئی کرنے کے لیے۔
اعصابی نیٹ ورکس، سپورٹ ویکٹر مشینیں، اور بے ترتیب جنگلات مشین سیکھنے کے مزید طریقوں میں شامل ہیں جو پروٹین کی ساخت کی پیشن گوئی کرنے کا وعدہ ظاہر کرتے ہیں۔
یہ الگورتھم بہت زیادہ ڈیٹاسیٹس سے سیکھ سکتے ہیں۔ اور، وہ مختلف امینو ایسڈز کے درمیان ارتباط کا اندازہ لگا سکتے ہیں۔ تو، آئیے دیکھتے ہیں کہ یہ کیسے کام کرتا ہے۔

شریک ارتقائی تجزیے اور پہلی الفا فولڈ جنریشن
کی کامیابی الفا فولڈ ایک گہرے نیورل نیٹ ورک ماڈل پر بنایا گیا ہے جو شریک ارتقائی تجزیہ کو استعمال کرتے ہوئے تیار کیا گیا ہے۔ شریک ارتقاء کا تصور یہ بتاتا ہے کہ اگر ایک پروٹین میں دو امینو ایسڈ ایک دوسرے کے ساتھ بات چیت کرتے ہیں، تو وہ اپنے فعال ربط کو برقرار رکھنے کے لیے ایک ساتھ ترقی کریں گے۔
محققین متعدد ملتے جلتے پروٹینوں کے امینو ایسڈ کی ترتیب کا موازنہ کرکے یہ پتہ لگاسکتے ہیں کہ 3D ڈھانچے میں امینو ایسڈ کے کون سے جوڑے رابطے میں ہیں۔
یہ ڈیٹا الفا فولڈ کے پہلے تکرار کی بنیاد کے طور پر کام کرتا ہے۔ یہ امینو ایسڈ کے جوڑوں کے ساتھ ساتھ پیپٹائڈ بانڈز کے زاویوں کے درمیان لمبائی کی پیش گوئی کرتا ہے جو ان کو جوڑتے ہیں۔ اس طریقہ کار نے تسلسل سے پروٹین کے ڈھانچے کی پیشن گوئی کرنے کے لیے تمام پیشگی طریقوں سے بہتر کارکردگی کا مظاہرہ کیا، حالانکہ درستگی ابھی تک ان پروٹینوں کے لیے محدود تھی جس میں کوئی واضح ٹیمپلیٹس نہیں تھے۔

الفا فولڈ 2: ایک بالکل نیا طریقہ کار
AlphaFold2 ایک کمپیوٹر سافٹ ویئر ہے جسے DeepMind نے بنایا ہے جو پروٹین کی 3D ساخت کی پیش گوئی کرنے کے لیے ایک پروٹین کے امینو ایسڈ کی ترتیب کا استعمال کرتا ہے۔
یہ اہم ہے کیونکہ پروٹین کا ڈھانچہ یہ بتاتا ہے کہ یہ کیسے کام کرتا ہے، اور اس کے کام کو سمجھنے سے سائنسدانوں کو پروٹین کو نشانہ بنانے والی ادویات تیار کرنے میں مدد مل سکتی ہے۔
الفا فولڈ 2 نیورل نیٹ ورک پروٹین کے امینو ایسڈ کی ترتیب کو ان پٹ کے طور پر حاصل کرتا ہے اور ساتھ ہی اس بارے میں تفصیلات بھی کہ وہ ترتیب ڈیٹا بیس میں موجود دیگر ترتیبوں سے کیسے موازنہ کرتی ہے (اسے "سلسلہ سیدھ" کہا جاتا ہے)۔
عصبی نیٹ ورک اس ان پٹ کی بنیاد پر پروٹین کی 3D ساخت کے بارے میں پیشین گوئی کرتا ہے۔
AlphaFold2 کے علاوہ اسے کیا سیٹ کرتا ہے؟
دوسرے طریقوں کے برعکس، الفا فولڈ 2 پروٹین کے حقیقی 3D ڈھانچے کی پیش گوئی کرتا ہے نہ کہ صرف امینو ایسڈ کے جوڑوں کے درمیان علیحدگی یا ان کو جوڑنے والے بانڈز کے درمیان زاویوں کی (جیسا کہ پہلے الگورتھم کرتا تھا)۔
عصبی نیٹ ورک کے لیے ایک ہی وقت میں مکمل ڈھانچے کا اندازہ لگانے کے لیے، ساخت کو آخر سے آخر تک انکوڈ کیا جاتا ہے۔
AlphaFold2 کی ایک اور اہم خصوصیت یہ ہے کہ یہ اندازہ پیش کرتا ہے کہ یہ اپنی پیشن گوئی میں کتنا پراعتماد ہے۔ یہ متوقع ڈھانچے پر ایک کلر کوڈنگ کے طور پر پیش کیا جاتا ہے، جس میں سرخ رنگ زیادہ اعتماد کی نمائندگی کرتا ہے اور نیلے رنگ کم اعتماد کی تجویز کرتا ہے۔
یہ مفید ہے کیونکہ یہ سائنسدانوں کو پیشین گوئی کے استحکام سے آگاہ کرتا ہے۔
کئی ترتیبوں کے مشترکہ ڈھانچے کی پیش گوئی کرنا
Alphafold2 کی تازہ ترین توسیع، جسے Alphafold Multimer کہا جاتا ہے، کئی ترتیبوں کے مشترکہ ڈھانچے کی پیش گوئی کرتا ہے۔ اس میں اب بھی اعلی غلطی کی شرح ہے یہاں تک کہ اگر یہ پہلے کی تکنیکوں سے کہیں بہتر کارکردگی کا مظاہرہ کرتی ہے۔ 25 پروٹین کمپلیکس میں سے صرف %4500 کی کامیابی سے پیش گوئی کی گئی۔
رابطے کی تشکیل کے کھردرے علاقوں میں سے 70٪ کی صحیح پیش گوئی کی گئی تھی، لیکن دونوں پروٹینوں کی نسبتی واقفیت غلط تھی۔ جب درمیانی صف بندی کی گہرائی تقریباً 30 ترتیبوں سے کم ہوتی ہے، تو الفافولڈ ملٹیمر پیشین گوئیوں کی درستگی نمایاں طور پر کم ہو جاتی ہے۔
الفافولڈ پیشن گوئیوں کا استعمال کیسے کریں۔
AlphaFold سے پیش گوئی شدہ ماڈل ایک ہی فائل فارمیٹس میں پیش کیے جاتے ہیں اور تجرباتی ڈھانچے کی طرح استعمال کیے جا سکتے ہیں۔ غلط فہمیوں کو روکنے کے لیے ماڈل کے ساتھ پیش کردہ درستگی کے تخمینے کو مدنظر رکھنا بہت ضروری ہے۔
یہ خاص طور پر پیچیدہ ڈھانچے کے لیے مفید ہے جیسے کہ باہم بنے ہوئے ہومومر یا پروٹین جو صرف ایک کی موجودگی میں فولڈ ہوتے ہیں۔
نامعلوم ligand.
کچھ چیلنجز۔
پیشن گوئی شدہ ڈھانچے کو استعمال کرنے میں بنیادی مسئلہ حرکیات، لیگنڈ سلیکٹیویٹی، کنٹرول، ایلوسٹری، بعد از ترجمہ تبدیلیاں، اور پروٹین اور بائیو فزیکل ڈیٹا تک رسائی کے بغیر بائنڈنگ کے حرکیات کو سمجھنا ہے۔
مشین سیکھنے اور اس مسئلے پر قابو پانے کے لیے فزکس پر مبنی مالیکیولر ڈائنامکس ریسرچ کا استعمال کیا جا سکتا ہے۔
یہ تحقیقات خصوصی اور موثر کمپیوٹر فن تعمیر سے فائدہ اٹھا سکتی ہیں۔ اگرچہ الفا فولڈ نے پروٹین کے ڈھانچے کی پیش گوئی کرنے میں زبردست پیشرفت حاصل کی ہے، ساختی حیاتیات کے میدان میں ابھی بھی بہت کچھ سیکھنا باقی ہے، اور الفا فولڈ کی پیشن گوئیاں مستقبل کے مطالعے کا صرف نقطہ آغاز ہیں۔
دیگر قابل ذکر اوزار کیا ہیں؟
RoseTTAFold
RoseTTAFold، جسے واشنگٹن یونیورسٹی کے محققین نے بنایا ہے، اسی طرح پروٹین کے ڈھانچے کی پیشن گوئی کرنے کے لیے گہری سیکھنے کے الگورتھم کو بھی استعمال کرتا ہے، لیکن یہ پیش گوئی شدہ ڈھانچے کو بہتر بنانے کے لیے "ٹارشن اینگل ڈائنامکس سمولیشنز" کے نام سے جانا جاتا ایک نیا طریقہ بھی شامل کرتا ہے۔
اس طریقہ کار سے حوصلہ افزا نتائج برآمد ہوئے ہیں اور یہ موجودہ AI پروٹین فولڈنگ ٹولز کی حدود کو دور کرنے میں کارآمد ثابت ہو سکتا ہے۔
trRosetta
ایک اور ٹول، trRosetta، a کا استعمال کرکے پروٹین فولڈنگ کی پیش گوئی کرتا ہے۔ عصبی نیٹ ورک لاکھوں پروٹین کی ترتیب اور ڈھانچے پر تربیت یافتہ۔
یہ ایک "ٹیمپلیٹ پر مبنی ماڈلنگ" تکنیک کا بھی استعمال کرتا ہے تاکہ ٹارگٹ پروٹین کا تقابلی معلوم ڈھانچوں سے موازنہ کرکے زیادہ درست پیشین گوئیاں کی جاسکیں۔
یہ ثابت کیا گیا ہے کہ ٹرروسیٹا چھوٹے پروٹینوں اور پروٹین کمپلیکس کے ڈھانچے کی پیشن گوئی کرنے کے قابل ہے۔
DeepMetaPSICOV
DeepMetaPSICOV ایک اور ٹول ہے جو پروٹین کے رابطے کے نقشوں کی پیشن گوئی پر توجہ مرکوز کرتا ہے۔ یہ، پروٹین فولڈنگ کی پیشن گوئی کرنے کے لئے ایک رہنما کے طور پر استعمال ہوتے ہیں. یہ استعمال کرتا ہے۔ گہری سیکھنے ایک پروٹین کے اندر باقیات کے تعامل کے امکان کی پیش گوئی کرنے کے نقطہ نظر۔
یہ بعد میں رابطہ کے مجموعی نقشے کی پیش گوئی کے لیے استعمال ہوتے ہیں۔ DeepMetaPSICOV نے بڑی درستگی کے ساتھ پروٹین کے ڈھانچے کی پیشن گوئی کرنے کی صلاحیت ظاہر کی ہے، یہاں تک کہ جب پچھلے نقطہ نظر ناکام ہو گئے ہوں۔
مستقبل میں کیا انعقاد ہے؟
اے آئی پروٹین فولڈنگ کا مستقبل روشن ہے۔ گہری سیکھنے پر مبنی الگورتھم، خاص طور پر AlphaFold2، نے حال ہی میں پروٹین کے ڈھانچے کی قابل اعتماد پیشین گوئی کرنے میں بڑی پیش رفت کی ہے۔
اس دریافت میں سائنسدانوں کو پروٹین کی ساخت اور کام کو بہتر طور پر سمجھنے کی اجازت دے کر منشیات کی نشوونما کو تبدیل کرنے کی صلاحیت ہے، جو عام علاج کے اہداف ہیں۔
بہر حال، پروٹین کمپلیکس کی پیشن گوئی اور متوقع ڈھانچے کی حقیقی فعال حیثیت کا پتہ لگانے جیسے مسائل باقی ہیں۔ ان مسائل کو حل کرنے اور AI پروٹین فولڈنگ الگورتھم کی درستگی اور وشوسنییتا کو بڑھانے کے لیے مزید تحقیق کی ضرورت ہے۔
اس کے باوجود، اس ٹیکنالوجی کے ممکنہ فوائد بہت زیادہ ہیں، اور اس میں زیادہ موثر اور درست ادویات کی تیاری کی صلاحیت ہے۔





جواب دیجئے