Ce-ar fi dacă am putea folosi inteligența artificială pentru a răspunde unuia dintre cele mai mari mistere ale vieții – plierea proteinelor? Oamenii de știință lucrează la acest lucru de zeci de ani.
Mașinile pot prezice acum structurile proteinelor cu o precizie uimitoare folosind modele de învățare profundă, modificând dezvoltarea medicamentelor, biotehnologia și cunoștințele noastre despre procesele biologice fundamentale.
Vino alături de mine într-o explorare în domeniul intrigant al plierii proteinelor AI, unde tehnologia de ultimă oră se ciocnește de complexitatea vieții însăși.
Dezvăluirea misterului plierii proteinelor
Proteinele lucrează în corpul nostru ca niște mici mașini pentru a îndeplini sarcini cruciale, cum ar fi descompunerea alimentelor sau transportul oxigenului. Trebuie să fie pliate corect pentru ca acestea să funcționeze eficient, la fel cum o cheie trebuie tăiată corect pentru a se potrivi într-o broască. De îndată ce proteina este creată, începe un proces de pliere foarte complicat.
Plierea proteinelor este procesul prin care lanțurile lungi de aminoacizi, blocurile de construcție ale proteinei, se pliază în structuri tridimensionale care dictează funcția proteinei.
Luați în considerare un șir lung de margele care trebuie comandat într-o formă precisă; asta se întâmplă atunci când o proteină se pliază. Cu toate acestea, spre deosebire de margele, aminoacizii au caracteristici unice și interacționează între ei în diferite moduri, făcând plierea proteinelor un proces complex și sensibil.
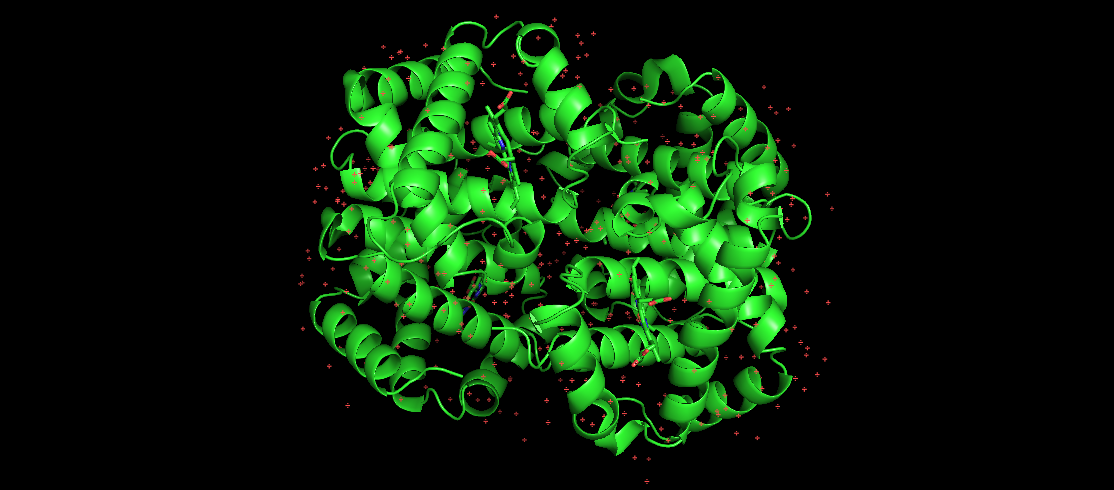
Imaginea de aici reprezintă hemoglobina umană, care este o proteină pliată bine-cunoscută
Proteinele trebuie să se plieze rapid și precis, altfel vor deveni pliate greșit și vor deveni defecte. Acest lucru ar putea duce la boli precum Alzheimer și Parkinson. Temperatura, presiunea și prezența altor molecule în celulă au toate un efect asupra procesului de pliere.
După zeci de ani de cercetare, oamenii de știință încă încearcă să descopere exact cum se pliază proteinele.
Din fericire, progresele în inteligența artificială îmbunătățesc dezvoltarea în sector. Oamenii de știință pot anticipa structura proteinelor cu mai multă acuratețe decât oricând prin utilizarea algoritmi de învățare automată pentru a examina volume masive de date.
Acest lucru are potențialul de a schimba dezvoltarea medicamentelor și de a crește cunoștințele noastre moleculare despre boală.
Pot mașinile să funcționeze mai bine?
Tehnicile convenționale de pliere a proteinelor au limitări
Oamenii de știință au încercat să descopere plierea proteinelor de zeci de ani, dar complexitatea procesului a făcut din acest subiect un subiect provocator.
Abordările convenționale de predicție a structurii proteinelor folosesc o combinație de metodologii experimentale și modelare computerizată, cu toate acestea, toate aceste metode au dezavantaje.
Tehnicile experimentale precum cristalografia cu raze X și rezonanța magnetică nucleară (RMN) pot fi consumatoare de timp și costisitoare. Și, modelele computerizate se bazează uneori pe presupuneri simple, care pot duce la predicții eronate.
AI poate depăși aceste obstacole
Din fericire, inteligență artificială oferă o promisiune nouă pentru o predicție mai precisă și eficientă a structurii proteinelor. Algoritmii de învățare automată pot examina volume masive de date. Și descoperă modele pe care oamenii le-ar rata.
Acest lucru a dus la crearea de noi instrumente software și platforme capabile să prezică structura proteinelor cu o precizie de neegalat.
Cei mai promițători algoritmi de învățare automată pentru predicția structurii proteinelor
Sistemul AlphaFold construit de Google DeepMind echipa este una dintre cele mai promițătoare progrese în acest domeniu. A înregistrat progrese mari în ultimii ani prin utilizare algoritmi de învățare profundă pentru a prezice structura proteinelor pe baza secvențelor lor de aminoacizi.
Rețelele neuronale, mașinile vectoriale de sprijin și pădurile aleatorii sunt printre mai multe metode de învățare automată care arată promițătoare pentru prezicerea structurii proteinelor.
Acești algoritmi pot învăța din seturi de date enorme. Și, ei pot anticipa corelațiile dintre diferiți aminoacizi. Deci, să vedem cum funcționează.

Analize co-evolutive și prima generație AlphaFold
Succesul de AlphaFold este construit pe un model de rețea neuronală profundă care a fost dezvoltat utilizând analiza co-evoluționară. Conceptul de co-evoluție afirmă că, dacă doi aminoacizi dintr-o proteină interacționează unul cu celălalt, ei se vor dezvolta împreună pentru a-și păstra legătura funcțională.
Cercetătorii pot detecta ce perechi de aminoacizi sunt susceptibile de a fi în contact în structura 3D, comparând secvențele de aminoacizi ale numeroaselor proteine similare.
Aceste date servesc drept bază pentru prima iterație a AlphaFold. Acesta prezice lungimile dintre perechile de aminoacizi, precum și unghiurile legăturilor peptidice care le leagă. Această metodă a depășit toate abordările anterioare pentru prezicerea structurii proteinei din secvență, deși acuratețea a fost încă limitată pentru proteinele fără șabloane aparente.

AlphaFold 2: O metodologie radical nouă
AlphaFold2 este un software de calculator creat de DeepMind care folosește secvența de aminoacizi a unei proteine pentru a prezice structura 3D a proteinei.
Acest lucru este semnificativ deoarece structura unei proteine dictează modul în care funcționează, iar înțelegerea funcției sale poate ajuta oamenii de știință să dezvolte medicamente care vizează proteina.
Rețeaua neuronală AlphaFold2 primește ca intrare secvența de aminoacizi a proteinei, precum și detalii despre modul în care această secvență se compară cu alte secvențe dintr-o bază de date (aceasta se numește „aliniere a secvenței”).
Rețeaua neuronală face o predicție despre structura 3D a proteinei pe baza acestei intrări.
Ce îl diferențiază de AlphaFold2?
Spre deosebire de alte abordări, AlphaFold2 prezice structura 3D reală a proteinei, mai degrabă decât doar separarea dintre perechile de aminoacizi sau unghiurile dintre legăturile care le conectează (cum au făcut algoritmii anteriori).
Pentru ca rețeaua neuronală să anticipeze întreaga structură dintr-o dată, structura este codificată de la capăt la capăt.
O altă caracteristică cheie a AlphaFold2 este că oferă o estimare a gradului de încredere în prognoza sa. Acesta este prezentat ca un cod de culoare pe structura anticipată, cu roșu reprezentând încredere ridicată și albastru sugerând încredere scăzută.
Acest lucru este util, deoarece informează oamenii de știință despre stabilitatea predicției.
Prezicerea structurii combinate a mai multor secvențe
Cea mai recentă extindere a Alphafold2, cunoscută sub numele de Alphafold Multimer, prognozează structura combinată a mai multor secvențe. Are în continuare rate mari de greșeală, chiar dacă funcționează mult mai bine decât tehnicile anterioare. Doar % 25 din 4500 de complexe de proteine au fost prezise cu succes.
70% din regiunile brute de formare a contactului au fost corect prezise, dar orientarea relativă a celor două proteine a fost incorectă. Când adâncimea medie de aliniere este mai mică de aproximativ 30 de secvențe, precizia predicțiilor multimerului Alphafold scade semnificativ.
Cum să utilizați predicțiile Alphafold
Modelele prezise de la AlphaFold sunt oferite în aceleași formate de fișiere și pot fi utilizate în aceleași moduri ca și structurile experimentale. Este esențial să țineți cont de estimările de acuratețe oferite cu modelul pentru a preveni neînțelegerile.
Este util în special pentru structurile complicate, cum ar fi homomerii împletite sau proteinele care se pliază doar în prezența unui
ligand necunoscut.
Unele provocări
Principala problemă în utilizarea structurilor prezise este înțelegerea dinamicii, selectivității liganzilor, controlului, alosteriei, modificărilor post-translaționale și cineticii legării fără acces la proteine și date biofizice.
Invatare mecanica și cercetarea dinamicii moleculare bazată pe fizică poate fi utilizată pentru a depăși această problemă.
Aceste investigații pot beneficia de o arhitectură informatică specializată și eficientă. În timp ce AlphaFold a realizat progrese uriașe în predicția structurilor proteinelor, mai sunt multe de învățat în domeniul biologiei structurale, iar predicțiile AlphaFold sunt doar punctul de plecare pentru studii viitoare.
Care sunt alte instrumente remarcabile?
RoseTTAFold
RoseTTAFold, creat de cercetătorii de la Universitatea din Washington, folosește, de asemenea, algoritmi de învățare profundă pentru a prezice structurile proteinelor, dar integrează și o abordare nouă cunoscută sub numele de „simulări ale dinamicii unghiului de torsiune” pentru a îmbunătăți structurile prezise.
Această metodă a dat rezultate încurajatoare și poate fi utilă pentru a depăși limitările instrumentelor existente de pliere a proteinelor AI.
trRosetta
Un alt instrument, trRosetta, prezice plierea proteinelor folosind a rețele neuronale antrenat pe milioane de secvențe și structuri de proteine.
De asemenea, folosește o tehnică de „modelare pe bază de șablon” pentru a crea predicții mai precise, comparând proteina țintă cu structuri cunoscute comparabile.
S-a demonstrat că trRosetta este capabilă să prezică structurile proteinelor mici și ale complexelor proteice.
DeepMetaPSICOV
DeepMetaPSICOV este un alt instrument care se concentrează pe prezicerea hărților de contact cu proteine. Acestea sunt folosite ca ghid pentru a prezice plierea proteinelor. Folosește învățare profundă abordări pentru a prognoza probabilitatea interacțiunilor reziduurilor în interiorul unei proteine.
Acestea sunt ulterior utilizate pentru a prognoza harta generală a contactelor. DeepMetaPSICOV a demonstrat potențialul de a prezice structurile proteinelor cu mare acuratețe, chiar și atunci când abordările anterioare au eșuat.
Ce rezerva viitorul?
Viitorul plierii proteinelor AI este luminos. Algoritmii bazați pe învățarea profundă, în special AlphaFold2, au făcut recent progrese mari în predicția fiabilă a structurilor proteinelor.
Această descoperire are potențialul de a transforma dezvoltarea medicamentelor, permițând oamenilor de știință să înțeleagă mai bine structura și funcția proteinelor, care sunt ținte terapeutice comune.
Cu toate acestea, rămân probleme precum prognoza complexelor de proteine și detectarea stării funcționale reale a structurilor anticipate. Sunt necesare mai multe cercetări pentru a rezolva aceste probleme și pentru a crește acuratețea și fiabilitatea algoritmilor de pliere a proteinelor AI.
Cu toate acestea, beneficiile potențiale ale acestei tehnologii sunt enorme și are potențialul de a duce la producerea de medicamente mai eficiente și mai precise.





Lasă un comentariu