Forskere avslører de skjulte strukturene til materialer og biomolekyler ved hjelp av krystallografi og kryo-elektronmikroskopi (kryo-EM). Men ettersom disse disiplinene møter stadig økende komplikasjoner, har maskinlæring blitt en verdifull alliert.
I dette innlegget skal vi se på det fascinerende skjæringspunktet mellom "Metodes of Machine Learning for Crystallography and Cryo-EM." Bli med oss mens vi undersøker den revolusjonerende virkningen av kunstig intelligens for å avdekke hemmelighetene til atom- og molekyluniversene.
Først av alt vil jeg lette inn på emnet og nevne hva som er vilkårene for krystallografi og Cryo-Em, så vil vi undersøke nærmere hvor maskinlæring kommer inn i stykket.
krystallografi
Krystallografi er studiet av arrangementet av atomer i krystallinske materialer. Krystaller er faste stoffer som består av atomer som er ordnet i et repeterende mønster for å danne en svært strukturert struktur.
På grunn av dette vanlige arrangementet har materialer unike egenskaper og oppførsel, noe som gjør krystallografi avgjørende for å forstå egenskapene til mange stoffer.
Forskere kan undersøke krystallgitteret ved hjelp av teknikker som røntgendiffraksjon, og gir viktig informasjon om atomposisjoner og bindingsinteraksjoner. Krystallografi er viktig på mange felt, fra materialvitenskap og kjemi til geologi og biologi. Det hjelper med utvikling av nye materialer og forståelse av mineralegenskaper.
Det kan til og med hjelpe oss med å tyde de kompliserte strukturene til biologiske molekyler som proteiner.
Cryo-EM (Cryo-Electron Microscopy)
Kryo-elektronmikroskopi (Cryo-EM) er en sofistikert bildeteknologi som lar forskere se de tredimensjonale strukturene til biomolekyler ved atomær eller nær-atomær oppløsning.
Cryo-EM bevarer biomolekyler i deres nesten naturlige tilstand ved å hurtigfryse dem i flytende nitrogen, i motsetning til standard elektronmikroskopi, som krever at prøver fikseres, farges og dehydreres.
Dette forhindrer iskrystalldannelse og bevarer biologisk struktur. Forskere kan nå se nøyaktige detaljer om enorme proteinkomplekser, virus og cellulære organeller, og gir avgjørende innsikt i deres funksjoner og forhold.
Cryo-EM har transformert strukturbiologien ved å la forskere utforske biologiske prosesser på tidligere utenkelige detaljnivåer. Dens anvendelser spenner fra medikamentoppdagelse og vaksineutvikling til å forstå sykdomsmolekylære grunnlag.
Hvorfor er de viktige?
Kryo-EM og krystallografi er avgjørende for å fremme vår forståelse av den naturlige verden.
Krystallografi gjør oss i stand til å oppdage og forstå atomarrangementet i materialer, noe som lar oss bygge nye forbindelser med spesifikke kvaliteter for et bredt spekter av bruksområder. Krystallografi er avgjørende for å forme vår moderne kultur, fra halvledere brukt i elektronikk til medisiner som brukes til å behandle plager.
Cryo-EM, derimot, gir et fascinerende innblikk i livets kompliserte mekanisme. Forskere får innsikt i grunnleggende biologiske prosesser ved å se på arkitekturen til biomolekyler, slik at de kan produsere bedre medisiner, designe målrettede terapier og effektivt bekjempe infeksjonssykdommer.
Cryo-EM-fremskritt åpner for nye utsikter innen medisin, bioteknologi og vår generelle forståelse av livets byggesteiner.
Forbedre strukturprediksjon og -analyse med maskinlæring i krystallografi
Maskinlæring har vært utrolig nyttig i krystallografi, og revolusjonerte hvordan forskere forutsier og tolker krystallstrukturer.
Algoritmer kan trekke ut mønstre og korrelasjoner fra enorme datasett med kjente krystallstrukturer, noe som muliggjør rask prediksjon av nye krystallstrukturer med uovertruffen presisjon.
For eksempel har Thorn Lab-forskere bevist effektiviteten til maskinlæring når det gjelder å forutsi krystallstabilitet og formasjonsenergi, og gir viktig innsikt i de termodynamiske egenskapene til materialer.
Denne utviklingen akselererer ikke bare oppdagelsen av nye materialer, men også optimaliseringen av dagens, og bringer inn en ny æra av materialforskning med bedre kvaliteter og funksjonalitet.
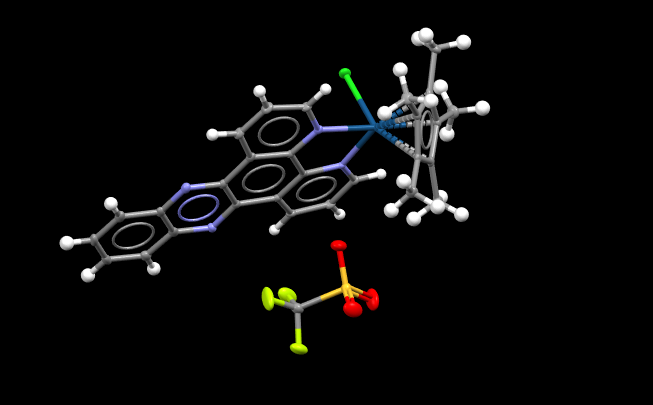
Bilde: Et eksempel på en krystallstruktur illustrert på Mercury-programvaren.
Hvordan avduker maskinlæring Cryo-EM?
Maskinlæring har åpnet opp en ny verden av muligheter innen kryo-elektronmikroskopi (Cryo-EM), slik at forskere kan fordype seg dypere i den strukturelle kompleksiteten til biomolekyler.
Forskere kan analysere enorme mengder kryo-EM-data ved å bruke nye teknologier som f.eks dyp læring, rekonstruere tredimensjonale modeller av biologiske molekyler med uovertruffen klarhet og nøyaktighet.
Denne kombinasjonen av maskinlæring med cryo-EM har muliggjort avbildning av tidligere udefinerbare proteinstrukturer, og gir ny innsikt i deres aktiviteter og relasjoner.
Kombinasjonen av disse teknologiene gir et enormt løfte for medisinoppdagelse siden den lar forskere målrette nøyaktig mot spesifikke bindingssteder, noe som fører til etableringen av mer effektive medisiner for en rekke lidelser.
Maskinlæringsalgoritmer for akselererende Cryo-EM-dataanalyse
Cryo-EM-undersøkelser genererer detaljerte og massive datasett, som kan være både en gave og en forbannelse for forskere. Maskinlæringsmetoder har imidlertid vist seg å være avgjørende for effektiv analyse og tolkning av kryo-EM-data.
Forskere kan bruke uovervåkede læringsmetoder for automatisk å oppdage og klassifisere ulike proteinstrukturer, noe som reduserer de tidkrevende manuelle operasjonene.
Denne metoden øker ikke bare dataanalysen raskere, men forbedrer også funnens pålitelighet ved å fjerne menneskelige skjevheter i tolkningen av kompliserte strukturelle data.
Inkorporeringen av maskinlæring i Cryo-EM-dataanalyse, som demonstrert i nyere arbeider, tilbyr en måte for en dypere kunnskap om kompliserte biologiske prosesser og en mer grundig undersøkelse av livets molekylære maskineri.
Mot hybride tilnærminger: bygge bro mellom eksperiment-beregningsgapet
Maskinlæring har potensial til å bygge bro mellom eksperimentelle data og beregningsmodeller innen krystallografi og kryo-EM.
Kombinasjonen av eksperimentelle data og maskinlæringsteknikker muliggjør utvikling av presise prediktive modeller, noe som forbedrer påliteligheten til strukturbestemmelse og egenskapsestimat.
Overføringslæring, en teknikk som anvender kunnskap lært på ett område til et annet, fremstår som et viktig verktøy for å øke effektiviteten til krystallografiske og Cryo-EM-undersøkelser i denne sammenhengen.
Hybride teknikker, som kombinerer eksperimentell innsikt med datamaskinkapasitet, representerer et banebrytende alternativ for å løse utfordrende vitenskapelige utfordringer, og lover å endre hvordan vi ser og manipulerer den atomære og molekylære verdenen.
Bruke konvolusjonelle nevrale nettverk for å plukke partikler i Cryo-EM
Ved å gi høyoppløselige bilder av biologiske molekyler, har kryo-elektronmikroskopi (Cryo-EM) transformert studiet av makromolekylære strukturer.
Imidlertid har partikkelplukking, som innebærer å gjenkjenne og trekke ut individuelle partikkelbilder fra Cryo-EM-mikrografer, en tidkrevende og vanskelig oppgave.
Forskere har gjort enorme fremskritt med å automatisere denne prosedyren med bruk av maskinlæring, spesielt konvolusjonelle nevrale nettverk (CNN).
DeepPicker og Topaz-Denoise er to dyp læringsalgoritmer som muliggjør helautomatisert partikkelutvelgelse i cryo-EM, noe som øker betydelig hastighet på databehandling og analyse.
CNN-baserte tilnærminger har blitt kritiske for å fremskynde Cryo-EM-prosedyrer og la forskere fokusere på undersøkelser på høyere nivå ved nøyaktig å detektere partikler med høy presisjon.
Optimalisering av krystallografi ved bruk av prediktiv modellering
Kvaliteten på diffraksjonsdata og krystalliseringsresultater kan ha en betydelig innvirkning på strukturbestemmelse i makromolekylær krystallografi.
Kunstige nevrale nettverk (ANN) og støttevektormaskiner (SVM) har blitt brukt med hell for å optimalisere krystalliseringsinnstillinger og forutsi krystalldiffraksjonskvalitet. Prediktive modeller produsert av forskere hjelper til med utformingen av eksperimenter og øker suksessraten for krystalliseringsforsøk.
Disse modellene kan avdekke mønstre som fører til gode resultater ved å evaluere enorme mengder krystalliseringsdata, og hjelpe forskere med å produsere krystaller av høy kvalitet for påfølgende røntgendiffraksjonstester. Som et resultat har maskinlæring blitt et uunnværlig verktøy for rask og målrettet krystallografisk testing.
Forbedring av Cryo-EM strukturell gjenkjennelse
Å forstå den sekundære strukturen til biologiske molekyler ved bruk av Cryo-EM-tetthetskart er avgjørende for å bestemme funksjonene og interaksjonene deres.
Maskinlæringsmetoder, nemlig dyplæringsarkitekturer som grafkonvolusjonelle og tilbakevendende nettverk, har blitt brukt for å lokalisere sekundære strukturfunksjoner i cryo-EM-kart automatisk.
Disse metodene undersøker lokale trekk i tetthetskart, noe som muliggjør presis klassifisering av sekundære strukturelle elementer. Maskinlæring gjør det mulig for forskere å undersøke kompliserte kjemiske strukturer og skaffe seg innsikt i deres biologiske aktiviteter ved å automatisere denne arbeidskrevende prosessen.

Bilde: Cryo-EM rekonstituering av en struktur
Krystallografi modellbygging og valideringsakselerasjon
Modellkonstruksjon og validering er nøkkelfaser i makromolekylær krystallografi for å sikre strukturell modellnøyaktighet og pålitelighet.
Maskinlæringsteknologier som konvolusjonelle autoenkodere og Bayesianske modeller har blitt brukt for å hjelpe og forbedre disse prosessene. AAnchor, for eksempel, bruker CNN-er for å gjenkjenne ankeraminosyrer i Cryo-EM-tetthetskart, noe som hjelper til med automatisk modellutvikling.
Bayesianske maskinlæringsmodeller ble også brukt til å integrere røntgendiffraksjonsdata og tilordne romgrupper i elektrontetthetskart for små molekyler.
Disse fremskrittene øker ikke bare strukturbestemmelsen, men gir også mer omfattende vurderinger av modellkvalitet, noe som resulterer i mer robuste og reproduserbare forskningsresultater.
Maskinlærings fremtid i strukturbiologi
Som sett av det økende antallet vitenskapelige publikasjoner, blir integreringen av maskinlæring i kryo-EM og krystallografi stadig bedre, og gir en mengde nye løsninger og applikasjoner.
Maskinlæring lover å forvandle det strukturelle biologimiljøet ytterligere med kontinuerlig utvikling av kraftige algoritmer og utvidelse av kurerte ressurser.
Synergien mellom maskinlæring og strukturell biologi baner vei for oppdagelser og innsikt i atom- og molekylverdenen, fra rask strukturbestemmelse til medikamentoppdagelse og proteinutvikling.
Den pågående forskningen på dette fascinerende emnet inspirerer forskere til å utnytte kraften til AI og låse opp mysteriene til livets byggesteiner.
konklusjonen
Inkorporeringen av maskinlæringsteknologier i krystallografi og kryo-elektronmikroskopi har åpnet en ny tidsalder innen strukturbiologi.
Maskinlæring har fremskyndet forskningstempoet betydelig og brakt enestående innsikt i atom- og molekylverdenen, fra automatisering av krevende operasjoner som partikkelutvelgelse til forbedring av prediktiv modellering for krystallisering og diffraksjonskvalitet.
Forskere kan nå effektivt evaluere enorme mengder data ved hjelp av konvolusjon nevrale nettverk og andre avanserte algoritmer, som umiddelbart forutser krystallstrukturer og trekker ut verdifull informasjon fra tetthetskart for kryo-elektronmikroskopi.
Denne utviklingen fremskynder ikke bare eksperimentelle operasjoner, men gir også mulighet for en mer dyptgående studie av biologiske strukturer og funksjoner.
Til slutt endrer konvergensen av maskinlæring og strukturell biologi landskapene for krystallografi og kryo-elektronmikroskopi.
Sammen bringer disse banebrytende teknologiene oss nærmere en bedre forståelse av atom- og molekylverdenen, og lover spillskiftende gjennombrudd innen materialforskning, medisinutvikling og selve livets intrikate maskineri.
Når vi omfavner denne fascinerende nye grensen, skinner fremtiden for strukturell biologi med ubegrensede muligheter og evnen til å løse naturens vanskeligste gåter.





Legg igjen en kommentar