Што кога би можеле да ја искористиме вештачката интелигенција за да одговориме на една од најголемите животни мистерии – преклопувањето на протеините? Научниците работат на ова со децении.
Сега машините можат да предвидат протеински структури со неверојатна прецизност користејќи модели за длабоко учење, менување на развојот на лекови, биотехнологијата и нашето знаење за основните биолошки процеси.
Придружете ми се на истражување во интригантната област на виткање протеини со вештачка интелигенција, каде што врвната технологија се судира со сложеноста на самиот живот.
Откривање на мистеријата за превиткување на протеини
Протеините работат во нашите тела како мали машини за извршување на клучни задачи како разградување на храната или транспорт на кислород. Тие мора да се преклопат правилно за да функционираат ефикасно, исто како што клучот мора правилно да се сече за да се вклопи во бравата. Штом се создаде протеинот, започнува многу комплициран процес на превиткување.
Преклопување на протеини е процес со кој долгите синџири на аминокиселини, градежните блокови на протеинот, се преклопуваат во тридимензионални структури кои ја диктираат функцијата на протеинот.
Размислете за долга низа од монистра што мора да се нарачаат во прецизна форма; тоа е она што се случува кога протеинот се преклопува. Сепак, за разлика од зрната, амино киселините имаат уникатни карактеристики и комуницираат една со друга на различни начини, што го прави преклопувањето на протеините сложен и чувствителен процес.
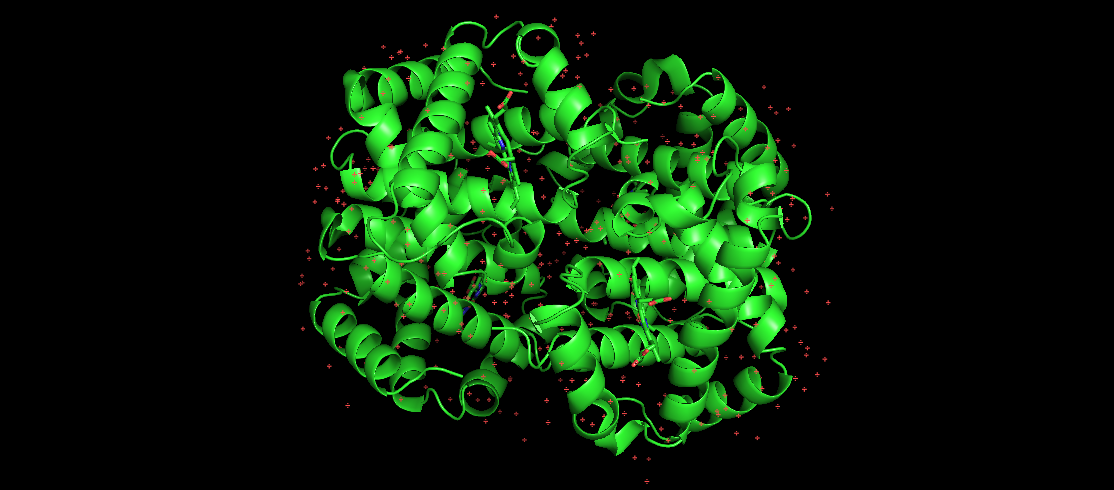
Сликата овде го претставува човечкиот хемоглобин, кој е добро познат преклопен протеин
Протеините мора да се преклопат брзо и прецизно, или ќе станат погрешно преклопени и неисправни. Тоа може да доведе до болести како што се Алцхајмерова и Паркинсонова болест. Температурата, притисокот и присуството на други молекули во ќелијата имаат влијание врз процесот на превиткување.
По децении истражување, научниците сè уште се обидуваат да откријат како точно се преклопуваат протеините.
За среќа, напредокот во вештачката интелигенција го подобрува развојот во секторот. Научниците можат да ја предвидат структурата на протеините попрецизно од кога било досега со користење алгоритми за машинско учење да се испитаат огромни количини на податоци.
Ова има потенцијал да го промени развојот на лекови и да го зголеми нашето молекуларно знаење за болеста.
Дали машините можат да работат подобро?
Конвенционалните техники за преклопување на протеини имаат ограничувања
Научниците со децении се обидуваат да го откријат преклопувањето на протеините, но сложеноста на процесот ја направи оваа тема предизвикувачка.
Конвенционалните пристапи за предвидување на структурата на протеините користат комбинација од експериментални методологии и компјутерско моделирање, меѓутоа, сите овие методи имаат недостатоци.
Експерименталните техники како што се рендгенската кристалографија и нуклеарната магнетна резонанца (НМР) може да одземат време и скапи. И, компјутерските модели понекогаш се потпираат на едноставни претпоставки, што може да доведе до погрешни предвидувања.
Вештачката интелигенција може да ги надмине овие пречки
Среќно, вештачка интелигенција дава свежо ветување за попрецизно и поефикасно предвидување на структурата на протеините. Алгоритмите за машинско учење можат да испитаат огромни количини на податоци. И, тие откриваат шаблони што луѓето би ги пропуштиле.
Ова резултираше со создавање на нови софтверски алатки и платформи способни да ја предвидат структурата на протеините со неспоредлива прецизност.
Најперспективните алгоритми за машинско учење за предвидување на структурата на протеините
Системот AlphaFold изграден од Google Deepmind тимот е еден од најперспективните достигнувања во оваа област. Во последниве години постигна голем напредок со користење алгоритми за длабоко учење да се предвиди структурата на протеините врз основа на нивните аминокиселински секвенци.
Невронските мрежи, векторските машини за поддршка и случајните шуми се меѓу повеќе методи за машинско учење кои ветуваат за предвидување на структурата на протеините.
Овие алгоритми можат да учат од огромни збирки на податоци. И, тие можат да ги предвидат корелациите помеѓу различните амино киселини. Значи, да видиме како функционира.

Ко-еволутивни анализи и првата генерација на алфафолд
Успехот на AlphaFold е изграден на модел на длабока невронска мрежа кој е развиен користејќи ко-еволутивна анализа. Концептот на ко-еволуција вели дека ако две аминокиселини во протеинот комуницираат една со друга, тие ќе се развијат заедно за да ја задржат својата функционална врска.
Истражувачите можат да откријат кои парови на амино киселини најверојатно ќе бидат во допир во 3D структурата со споредување на секвенците на аминокиселини на бројни слични протеини.
Овие податоци служат како основа за првата итерација на AlphaFold. Ги предвидува должините помеѓу паровите на амино киселините, како и аглите на пептидните врски што ги поврзуваат. Овој метод ги надмина сите претходни пристапи за предвидување на структурата на протеините од низата, иако точноста беше сè уште ограничена за протеините без очигледни шаблони.

АлфаФолд 2: Радикално нова методологија
AlphaFold2 е компјутерски софтвер создаден од DeepMind кој користи аминокиселинска секвенца на протеин за да ја предвиди 3D структурата на протеинот.
Ова е значајно бидејќи структурата на протеинот диктира како функционира, а разбирањето на неговата функција може да им помогне на научниците да развијат лекови кои го таргетираат протеинот.
Невралната мрежа AlphaFold2 како влез ја прима амино киселинската секвенца на протеинот, како и детали за тоа како таа низа се споредува со другите секвенци во базата на податоци (ова се нарекува „порамнување на секвенцата“).
Невралната мрежа прави предвидување за 3Д структурата на протеинот врз основа на овој влез.
Што го издвојува од AlphaFold2?
За разлика од другите пристапи, AlphaFold2 ја предвидува вистинската 3D структура на протеинот наместо само одвојување помеѓу паровите на амино киселини или аглите помеѓу врските што ги поврзуваат (како што правеа претходните алгоритми).
Со цел невронската мрежа да ја предвиди целосната структура одеднаш, структурата е кодирана од крај до крај.
Друга клучна карактеристика на AlphaFold2 е тоа што нуди проценка за тоа колку е сигурен во својата прогноза. Ова е претставено како кодирање во боја на предвидената структура, при што црвеното претставува висока доверба, а синото сугерира ниска доверба.
Ова е корисно бидејќи ги информира научниците за стабилноста на предвидувањето.
Предвидување на комбинираната структура на неколку секвенци
Најновата експанзија на Alphafold2, позната како Alphafold Multimer, предвидува комбинирана структура на неколку секвенци. Сè уште има високи стапки на грешки, дури и ако работи многу подобро од претходните техники. Само 25% од 4500 протеински комплекси беа успешно предвидени.
70% од грубите области на формирање на контакт беа точно предвидени, но релативната ориентација на двата протеини беше неточна. Кога просечната длабочина на порамнување е помала од приближно 30 секвенци, точноста на предвидувањата на мултимерот Alphafold значително опаѓа.
Како да користите алфафолд предвидувања
Предвидените модели од AlphaFold се нудат во исти формати на датотеки и може да се користат на исти начини како и експерименталните структури. Од клучно значење е да се земат предвид проценките за точноста понудени со моделот за да се спречат недоразбирања.
Тој е особено корисен за комплицирани структури како што се испреплетени хомомери или протеини кои се преклопуваат само во присуство на
непознат лиганд.
Некои предизвици
Главниот проблем во користењето на предвидените структури е разбирањето на динамиката, селективноста на лигандот, контролата, алостеријата, пост-преведувачките промени и кинетиката на врзувањето без пристап до протеини и биофизички податоци.
Машинско учење и истражувањето за молекуларна динамика базирано на физика може да се искористи за да се надмине овој проблем.
Овие истраги може да имаат корист од специјализирана и ефикасна компјутерска архитектура. Додека AlphaFold постигна огромен напредок во предвидувањето на протеинските структури, има уште многу да се научи во областа на структурната биологија, а предвидувањата на AlphaFold се само почетна точка за идното проучување.
Кои се другите извонредни алатки?
RoseTTAFold
RoseTTAFold, создаден од истражувачите од Универзитетот во Вашингтон, исто така користи алгоритми за длабоко учење за да ги предвиди протеинските структури, но исто така интегрира нов пристап познат како „симулации на динамика на аголот на торзија“ за подобрување на предвидените структури.
Овој метод даде охрабрувачки резултати и може да биде корисен за надминување на ограничувањата на постоечките алатки за виткање протеини со вештачка интелигенција.
trРозета
Друга алатка, trRosetta, предвидува преклопување на протеините со користење на a невронска мрежа обучени на милиони протеински секвенци и структури.
Исто така, користи техника „моделирање базирано на шаблони“ за да создаде попрецизни предвидувања со споредување на целниот протеин со споредливи познати структури.
Докажано е дека trRosetta е способна да ги предвиди структурите на ситни протеини и протеински комплекси.
DeepMetaPSICOV
DeepMetaPSICOV е уште една алатка која се фокусира на предвидување на мапи за контакт со протеини. Тие се користат како водич за предвидување на виткање на протеини. Таа користи длабоко учење пристапи за прогноза на веројатноста за интеракции на остатоци во протеинот.
Тие потоа се користат за прогнозирање на целокупната контактна карта. DeepMetaPSICOV покажа потенцијал во предвидување на протеинските структури со голема точност, дури и кога претходните пристапи не успеаја.
Што носи иднината?
Иднината на виткањето на протеини со вештачка интелигенција е светла. Алгоритмите засновани на длабоко учење, особено AlphaFold2, неодамна постигнаа голем напредок во веродостојното предвидување на протеинските структури.
Ова откритие има потенцијал да го трансформира развојот на лекови со тоа што ќе им овозможи на научниците подобро да ја разберат структурата и функцијата на протеините, кои се вообичаени терапевтски цели.
Сепак, остануваат прашањата како прогнозирање на протеинските комплекси и откривање на реалниот функционален статус на очекуваните структури. Потребни се повеќе истражувања за да се решат овие прашања и да се зголеми точноста и веродостојноста на алгоритмите за виткање протеини со вештачка интелигенција.
Сепак, потенцијалните придобивки од оваа технологија се огромни и има потенцијал да доведе до производство на поефикасни и попрецизни лекови.





Оставете Одговор