Wat wa mir kënschtlech Intelligenz benotze fir ee vun de gréisste Mystère vum Liewen ze beäntweren - Proteinfolding? D'Wëssenschaftler schaffe schonn zënter Joerzéngte drun.
Maschinnen kënnen elo Proteinstrukturen mat erstaunlecher Präzisioun virauszesoen andeems déif Léiermodeller benotzt ginn, Drogenentwécklung, Biotechnologie an eist Wëssen iwwer fundamental biologesch Prozesser änneren.
Kommt mat mir op eng Exploratioun an dat faszinéierend Räich vun AI Proteinfolding, wou déi modernst Technologie mat der Komplexitéit vum Liewen selwer kollidéiert.
Entdeckt d'Mystère vum Protein Folding
Proteine funktionnéieren an eisem Kierper wéi kleng Maschinnen fir entscheedend Aufgaben auszeféieren wéi d'Liewensmëttel ofbriechen oder Sauerstoff transportéieren. Si musse richteg geklappt ginn fir datt se effektiv funktionnéieren, sou wéi e Schlëssel muss richteg geschnidden ginn fir an e Schloss ze passen. Soubal de Protein erstallt gëtt, fänkt e ganz komplizéierte Klappprozess un.
Proteinfolding ass de Prozess, duerch dee laang Ketten vun Aminosäuren, d'Bausteng vum Protein, an dreidimensional Strukturen falen, déi d'Funktioun vum Protein diktéieren.
Betruecht eng laang String vu Perlen, déi an enger präzis Form bestallt musse ginn; dat ass wat geschitt wann e Protein klappt. Wéi och ëmmer, am Géigesaz zu Perlen, hunn Aminosäuren eenzegaarteg Charakteristiken an interagéiere matenee op verschidde Manéieren, wat Proteinfolding zu engem komplexen a sensiblen Prozess mécht.
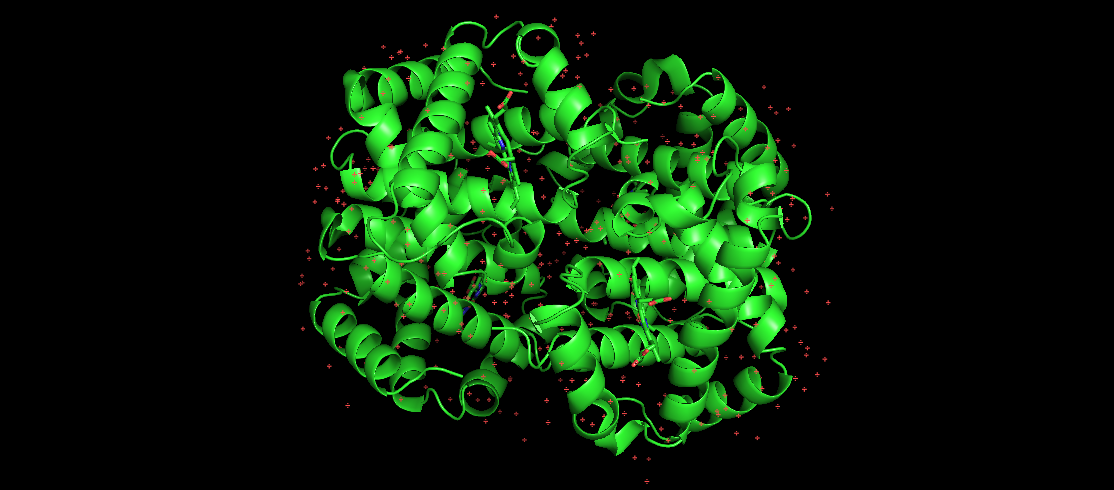
D'Bild hei representéiert mënschlecht Hämoglobin, wat e bekannte geklappte Protein ass
Proteine musse séier a präzis klappen, soss gi se falsch geklappt a defekt. Dat kéint zu Krankheeten wéi Alzheimer a Parkinson féieren. Temperatur, Drock an d'Präsenz vun anere Molekülen an der Zell hunn all en Effekt op de Klappprozess.
No Joerzéngte vu Fuerschung probéieren d'Wëssenschaftler nach ëmmer erauszefannen wéi d'Proteine sech klappen.
Glécklecherweis verbesseren Fortschrëtter an der kënschtlecher Intelligenz d'Entwécklung am Secteur. Wëssenschaftler kënnen d'Struktur vun Proteinen méi genee wéi jee viraus virauszegesinn andeems se benotzt Maschinn Léieren Algorithmen massive Volumen vun Donnéeën z'ënnersichen.
Dëst huet d'Potenzial fir d'Medikamententwécklung ze änneren an eist molekulare Wëssen iwwer d'Krankheet ze erhéijen.
Kënne Maschinnen besser Leeschtung?
Konventionell Protein Folding Techniken hunn Aschränkungen
D'Wëssenschaftler hu probéiert fir Joerzéngte Proteinfolden erauszefannen, awer d'Komplexitéit vum Prozess huet dëst zu engem Erausfuerderung Thema gemaach.
Konventionell Proteinstruktur Prognose Approche benotzen eng Kombinatioun vun experimentellen Methodologien a Computermodelléierung, awer dës Methoden hunn all Nodeeler.
Experimentell Techniken wéi Röntgenkristallographie an Nuklearmagnetesch Resonanz (NMR) kënnen ze laang an deier sinn. An, Computermodeller vertrauen heiansdo op einfache Viraussetzungen, wat zu falsche Prognosen féieren kann.
AI kann dës Hindernisser iwwerwannen
Gléck, Kënschtlech Intelligenz gëtt frësch Verspriechen fir méi genee an effizient Protein Struktur Viraussetzung. Maschinn Léieren Algorithmen kënne massiv Datenvolumen ënnersichen. An, si entdecken Musteren déi d'Leit verpassen.
Dëst huet zu der Schafung vun neie Software Tools a Plattformen gefouert, déi fäeg sinn d'Proteinstruktur mat onparalleléierter Präzisioun virauszesoen.
Déi verspriechendst Maschinnléieren Algorithmen fir Prognose vu Proteinstruktur
Den AlphaFold System gebaut vu Google Deepmind Team ass ee vun de villverspriechendste Fortschrëtter an dësem Beräich. Et huet grouss Fortschrëtter an de leschte Joeren duerch benotzt déif léieren Algorithmen d'Struktur vun Proteinen op Basis vun hiren Aminosaier Sequenzen virauszesoen.
Neural Netzwierker, Ënnerstëtzungsvektormaschinnen, an zoufälleg Bëscher gehéieren zu méi Maschinnléieremethoden déi Verspriechen weisen fir d'Proteinstruktur virauszesoen.
Dës Algorithmen kënnen aus enormen Datesätz léieren. An, si kënnen d'Korrelatiounen tëscht verschidden Aminosäuren viraussoen. Also, loosst eis kucken wéi et funktionnéiert.

Co-evolutionär Analysen an déi éischt AlphaFold Generatioun
Den Erfolleg vun AlphaFold ass op engem déiwe neuralen Netzwierkmodell gebaut deen entwéckelt gouf mat co-evolutionärer Analyse. D'Konzept vun der Co-Evolutioun seet datt wann zwou Aminosäuren an engem Protein matenee interagéieren, se zesumme entwéckelen fir hir funktionell Verbindung ze halen.
Fuerscher kënnen entdecken wéi eng Pairen vun Aminosäuren méiglecherweis an der 3D Struktur a Kontakt sinn, andeems d'Aminosäure Sequenze vu villen ähnlechen Proteinen vergläicht.
Dës Donnéeën déngen als Grondlag fir déi éischt Iteratioun vun AlphaFold. Et prognostizéiert d'Längt tëscht Aminosaierpaaren souwéi d'Wénkel vun de Peptidbindungen déi se verbannen. Dës Method huet all virdrun Approche fir d'Proteinstruktur aus der Sequenz virauszesoen, obwuel d'Genauegkeet nach ëmmer limitéiert war fir Proteinen ouni scheinbar Templates.

AlphaFold 2: Eng radikal nei Methodologie
AlphaFold2 ass eng Computersoftware erstallt vum DeepMind déi d'Aminosaier Sequenz vun engem Protein benotzt fir d'3D Struktur vum Protein virauszesoen.
Dëst ass bedeitend well d'Struktur vun engem Protein diktéiert wéi et funktionnéiert, a seng Funktioun ze verstoen kann d'Wëssenschaftler hëllefen Medikamenter z'entwéckelen déi de Protein zielen.
Den AlphaFold2 neuralen Netzwierk kritt als Input d'Aminosaier Sequenz vum Protein wéi och Detailer iwwer wéi dës Sequenz mat anere Sequenzen an enger Datebank vergläicht (dëst gëtt eng "Sequenz Ausrichtung" genannt).
Den neurale Netzwierk mécht eng Prognose iwwer d'3D Struktur vum Protein baséiert op dësem Input.
Wat ënnerscheet et vun AlphaFold2?
Am Géigesaz zu anere Approche virausgesot AlphaFold2 déi richteg 3D Struktur vum Protein anstatt nëmmen d'Trennung tëscht Pairen vun Aminosäuren oder d'Wénkel tëscht de Bindungen, déi se verbannen (wéi virdrun Algorithmen gemaach).
Fir datt den neurale Netzwierk déi voll Struktur gläichzäiteg virauszesoen, gëtt d'Struktur end-to-end kodéiert.
Eng aner Schlësselcharakteristik vum AlphaFold2 ass datt et eng Schätzung bitt wéi zouversiichtlech et a senger Prognose ass. Dëst gëtt als Faarfkodéierung op der virausgesoter Struktur presentéiert, mat rout representéiert héich Vertrauen a blo fir niddereg Vertrauen.
Dëst ass nëtzlech well et d'Wëssenschaftler iwwer d'Stabilitéit vun der Prognose informéiert.
Virauszesoen déi kombinéiert Struktur vu verschiddene Sequenzen
Déi lescht Expansioun vun Alphafold2, bekannt als Alphafold Multimer, prognostizéiert déi kombinéiert Struktur vu verschiddene Sequenzen. Et huet nach ëmmer héich Feelerraten och wann et vill besser funktionnéiert wéi fréier Techniken. Just %25 vu 4500 Proteinkomplexe goufen erfollegräich virausgesot.
70% vun de raue Regioune vun der Kontaktbildung ware richteg virausgesot, awer d'relativ Orientéierung vun den zwee Proteinen war falsch. Wann d'median Ausriichtungsdéift manner wéi ongeféier 30 Sequenzen ass, fällt d'Genauegkeet vun den Alphafold Multimer Prognosen bedeitend erof.
Wéi benotzen ech Alphafold Prognosen
Déi virausgesot Modeller vun AlphaFold ginn an déiselwecht Dateiformate ugebueden a kënnen op déiselwecht Manéier wéi experimentell Strukturen benotzt ginn. Et ass entscheedend d'Genauegkeetsschätzunge mat dem Modell ugebueden ze berücksichtegen fir Mëssverständnisser ze vermeiden.
Et ass besonnesch hëllefräich fir komplizéiert Strukturen wéi interwoven Homomeren oder Proteinen déi nëmmen an der Präsenz vun engem
onbekannt Ligand.
E puer Erausfuerderungen
Den Haaptproblem bei der Benotzung vun virausgesot Strukturen ass d'Dynamik ze verstoen, d'Ligand Selektivitéit, d'Kontroll, d'Allosterie, d'post-translational Verännerungen, an d'Kinetik vun der Bindung ouni Zougang zu Protein a biophysikaleschen Daten.
Machine learning a Physik-baséiert molekulare Dynamik Fuerschung ka benotzt ginn fir dëse Problem ze iwwerwannen.
Dës Ermëttlungen kënne vu spezialiséierter an effizienter Computerarchitektur profitéieren. Wärend AlphaFold enorm Fortschrëtter erreecht huet fir Proteinstrukturen virzebereeden, ass et nach vill ze léieren am Beräich vun der struktureller Biologie, an AlphaFold Prognosen sinn nëmmen den Ausgangspunkt fir zukünfteg Studie.
Wat sinn aner bemierkenswäert Tools?
RoseTTAFold
RoseTTAFold, erstallt vun der University of Washington Fuerscher, beschäftegt och déif Léieralgorithmen fir Proteinstrukturen virauszesoen, awer et integréiert och eng nei Approche bekannt als "Torsiounswinkel Dynamik Simulatioune" fir déi virausgesot Strukturen ze verbesseren.
Dës Method huet encouragéierend Resultater geliwwert a kann nëtzlech sinn fir d'Limitatioune vun existente AI Protein Klappinstrumenter ze iwwerwannen.
trRosetta
En anert Tool, trRosetta, virausgesot Proteinfolding mat engem neural Netz trainéiert op Millioune Proteinsequenzen a Strukturen.
Et benotzt och eng "Schabloun-baséiert Modeller" Technik fir méi präzis Prognosen ze kreéieren andeems de Zilprotein mat vergläichbare bekannte Strukturen vergläicht.
Et gouf bewisen datt trRosetta fäeg ass d'Strukturen vu klenge Proteinen a Proteinkomplexe virauszesoen.
DeepMetaPSICOV
DeepMetaPSICOV ass en anert Tool dat sech fokusséiert op d'Proteinkontaktkaarten virauszesoen. Dës ginn als Guide benotzt fir Proteinfolding virauszesoen. Et benotzt ze léieren Approche fir d'Wahrscheinlechkeet vu Reschtinteraktiounen bannent engem Protein virauszesoen.
Dës ginn duerno benotzt fir d'Gesamtkontaktkaart ze prognostizéieren. DeepMetaPSICOV huet Potenzial gewisen fir Proteinstrukturen mat grousser Genauegkeet virauszesoen, och wa fréier Approche gescheitert sinn.
Wéi gesäit d'Zukunft aus?
D'Zukunft vun AI Protein Folding ass hell. Deep Learning-baséiert Algorithmen, notamment AlphaFold2, hu viru kuerzem grousse Fortschrëtter gemaach fir zouverlässeg Proteinstrukturen virauszesoen.
Dës Entdeckung huet de Potenzial fir d'Drogenentwécklung ze transforméieren andeems d'Wëssenschaftler d'Struktur an d'Funktioun vu Proteinen besser verstoen, déi allgemeng therapeutesch Ziler sinn.
Trotzdem bleiwen Themen wéi d'Prognosen vu Proteinkomplexe an d'Erkennung vum realen funktionnelle Status vun viraussiichtleche Strukturen. Méi Fuerschung ass erfuerderlech fir dës Themen ze léisen an d'Genauegkeet an Zouverlässegkeet vun AI Protein Klappalgorithmen ze erhéijen.
Wéi och ëmmer, d'potenziell Virdeeler vun dëser Technologie sinn enorm, an et huet d'Potenzial fir méi effektiv a präzis Medikamenter ze produzéieren.





Hannerlooss eng Äntwert