מה אם נוכל להשתמש בבינה מלאכותית כדי לענות על אחת התעלומות הגדולות של החיים - קיפול חלבון? מדענים עובדים על זה כבר עשרות שנים.
מכונות יכולות כעת לחזות מבני חלבון בדיוק מדהים באמצעות מודלים של למידה עמוקה, שינוי פיתוח תרופות, ביוטכנולוגיה והידע שלנו על תהליכים ביולוגיים בסיסיים.
הצטרפו אליי לחקור את התחום המסקרן של קיפול חלבון AI, שבו טכנולוגיה חדשנית מתנגשת עם מורכבות החיים עצמם.
פותרים את המסתורין של קיפול חלבון
חלבונים פועלים בגופנו כמו מכונות קטנות לביצוע משימות חיוניות כמו פירוק מזון או הובלת חמצן. הם חייבים להיות מקופלים בצורה נכונה כדי שהם יתפקדו ביעילות, בדיוק כמו שמפתח צריך להיות חתוך נכון כדי להתאים למנעול. ברגע שנוצר החלבון מתחיל תהליך קיפול מסובך מאוד.
קיפול חלבון הוא התהליך שבו מתקפלות שרשראות ארוכות של חומצות אמינו, אבני הבניין של החלבון, למבנים תלת מימדיים המכתיבים את תפקוד החלבון.
שקול מחרוזת ארוכה של חרוזים שיש להזמין בצורה מדויקת; זה מה שקורה כאשר חלבון מתקפל. עם זאת, בניגוד לחרוזים, לחומצות אמינו יש מאפיינים ייחודיים והן מקיימות אינטראקציה זו עם זו בדרכים שונות, מה שהופך את קיפול החלבון לתהליך מורכב ורגיש.
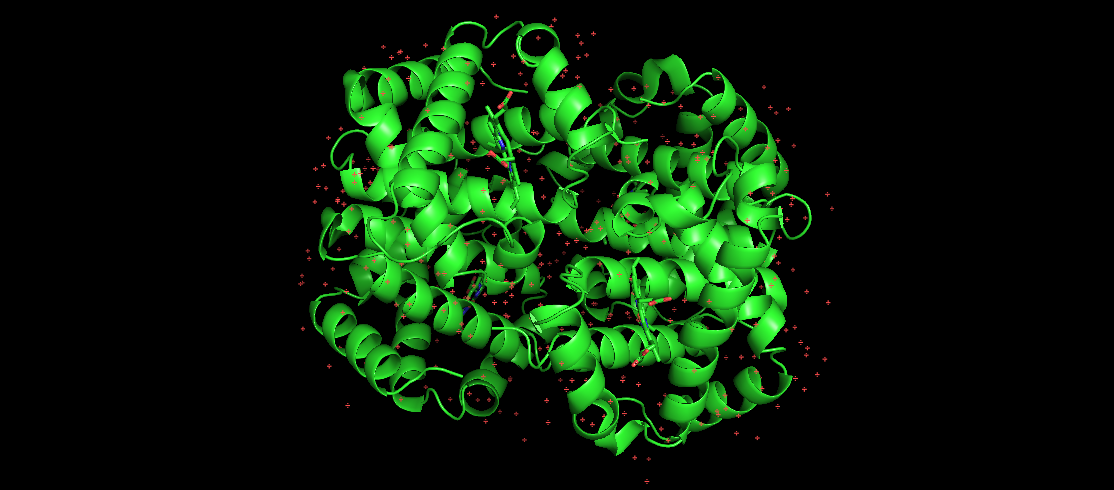
התמונה כאן מייצגת המוגלובין אנושי, שהוא חלבון מקופל ידוע
חלבונים חייבים להתקפל מהר ומדויק, אחרת הם יהפכו לא מקופלים ופגומים. זה עלול להוביל למחלות כמו אלצהיימר ופרקינסון. לטמפרטורה, ללחץ ולנוכחות של מולקולות אחרות בתא יש השפעה על תהליך הקיפול.
אחרי עשרות שנים של מחקר, מדענים עדיין מנסים להבין איך בדיוק חלבונים מתקפלים.
למרבה המזל, התקדמות בבינה מלאכותית משפרת את הפיתוח במגזר. מדענים יכולים לצפות את מבנה החלבונים בצורה מדויקת יותר מאי פעם על ידי שימוש אלגוריתמים למידת מכונה לבחון כמויות אדירות של נתונים.
יש לכך פוטנציאל לשנות את התפתחות התרופות ולהגדיל את הידע המולקולרי שלנו על המחלה.
האם מכונות יכולות להצליח יותר?
לטכניקות קיפול חלבון קונבנציונליות יש מגבלות
מדענים מנסים להבין את קיפול החלבון במשך עשרות שנים, אבל מורכבות התהליך הפכה את זה לנושא מאתגר.
גישות קונבנציונליות לחיזוי מבנה חלבון משתמשות בשילוב של מתודולוגיות ניסוי ומודלים ממוחשבים, אולם לשיטות אלו יש חסרונות.
טכניקות ניסוי כמו קריסטלוגרפיה של קרני רנטגן ותהודה מגנטית גרעינית (NMR) עשויות להיות גוזלות זמן ויקרות. כמו כן, מודלים ממוחשבים מסתמכים לפעמים על הנחות פשוטות, מה שעלול להוביל לתחזיות שגויות.
בינה מלאכותית יכולה להתגבר על המכשולים הללו
לְמַרְבֶּה הַמַזָל, בינה מלאכותית מספק הבטחה חדשה לחיזוי מדויק ויעיל יותר של מבנה חלבון. אלגוריתמים של למידת מכונה יכולים לבחון כמויות אדירות של נתונים. והם חושפים דפוסים שאנשים יחמיצו.
זה הביא ליצירת כלי תוכנה ופלטפורמות חדשות המסוגלות לחזות את מבנה החלבון בדיוק שאין שני לו.
האלגוריתמים המבטיחים ביותר ללימוד מכונה לחיזוי מבנה חלבון
מערכת AlphaFold שנבנתה על ידי גוגל Deepmind הצוות הוא אחד ההתקדמות המבטיחות ביותר בתחום זה. זה צבר התקדמות רבה בשנים האחרונות על ידי שימוש אלגוריתמי למידה עמוקים לחזות את מבנה החלבונים על סמך רצפי חומצות האמינו שלהם.
רשתות עצביות, מכונות וקטור תמיכה ויערות אקראיים הם בין שיטות למידת מכונה נוספות המראות הבטחה לניבוי מבנה חלבון.
אלגוריתמים אלה יכולים ללמוד ממערכי נתונים עצומים. בנוסף, הם יכולים לצפות את המתאמים בין חומצות אמינו שונות. אז בואו נראה איך זה עובד.

ניתוחים קו-אבולוציוניים ודור ה-AlphaFold הראשון
ההצלחה של AlphaFold בנוי על מודל רשת עצבית עמוקה שפותחה תוך שימוש בניתוח קו-אבולוציוני. הרעיון של אבולוציה משותפת קובע שאם שתי חומצות אמינו בחלבון יקיימו אינטראקציה זו עם זו, הן יתפתחו יחד כדי לשמור על הקשר התפקודי שלהן.
חוקרים יכולים לזהות אילו זוגות של חומצות אמינו צפויות להיות במגע במבנה התלת-ממדי על ידי השוואת רצפי חומצות האמינו של חלבונים דומים רבים.
נתונים אלה משמשים כבסיס לאיטרציה הראשונה של AlphaFold. הוא חוזה את האורכים בין זוגות חומצות אמינו וכן את הזוויות של קשרי הפפטידים המקשרים ביניהם. שיטה זו עלתה על כל הגישות הקודמות לניבוי מבנה חלבון מרצף, אם כי הדיוק עדיין היה מוגבל לחלבונים ללא תבניות נראות לעין.

AlphaFold 2: מתודולוגיה חדשה באופן קיצוני
AlphaFold2 היא תוכנת מחשב שנוצרה על ידי DeepMind המשתמשת ברצף חומצות אמינו של חלבון כדי לחזות את המבנה התלת מימדי של החלבון.
זה משמעותי מכיוון שמבנה החלבון מכתיב את אופן פעולתו, והבנת תפקידו יכולה לעזור למדענים לפתח תרופות המכוונות לחלבון.
הרשת העצבית AlphaFold2 מקבלת כקלט את רצף חומצות האמינו של החלבון וכן פרטים על איך רצף זה בהשוואה לרצפים אחרים במסד נתונים (זה נקרא "יישור רצף").
הרשת העצבית עושה חיזוי לגבי מבנה התלת-ממד של החלבון על סמך קלט זה.
מה מייחד אותו מ-AlphaFold2?
בניגוד לגישות אחרות, AlphaFold2 מנבא את המבנה התלת-ממדי האמיתי של החלבון ולא רק את ההפרדה בין זוגות של חומצות אמינו או את הזוויות בין הקשרים המחברים ביניהן (כפי שעשו אלגוריתמים קודמים).
על מנת שהרשת העצבית תצפה את המבנה המלא בבת אחת, המבנה מקודד מקצה לקצה.
מאפיין מרכזי נוסף של AlphaFold2 הוא שהוא מציע הערכה של כמה הוא בטוח בתחזית שלו. זה מוצג כקידוד צבע על המבנה הצפוי, כאשר אדום מייצג ביטחון גבוה וכחול מרמז על ביטחון נמוך.
זה שימושי מכיוון שהוא מודיע למדענים על יציבות התחזית.
חיזוי המבנה המשולב של מספר רצפים
ההרחבה האחרונה של Alphafold2, הידועה בשם Alphafold Multimer, חוזה את המבנה המשולב של מספר רצפים. עדיין יש לו שיעורי טעויות גבוהים גם אם הוא מתפקד הרבה יותר טוב מטכניקות קודמות. רק %25 מתוך 4500 קומפלקסים של חלבון נחזו בהצלחה.
70% מהאזורים הגסים של היווצרות מגע חזו נכון, אך הכיוון היחסי של שני החלבונים היה שגוי. כאשר עומק היישור החציוני הוא פחות מ-30 רצפים בערך, הדיוק של תחזיות מולטימר Alphafold יורד באופן משמעותי.
כיצד להשתמש בחיזוי Alphafold
המודלים החזויים של AlphaFold מוצעים באותם פורמטים של קבצים וניתן להשתמש בהם באותם דרכים כמו מבנים ניסיוניים. חשוב לקחת בחשבון את הערכות הדיוק המוצעות במודל על מנת למנוע אי הבנות.
זה מועיל במיוחד עבור מבנים מסובכים כמו הוממרים שזורים או חלבונים שמתקפלים רק בנוכחות
ליגנד לא ידוע.
כמה אתגרים
הבעיה העיקרית בשימוש במבנים חזויים היא הבנת הדינמיקה, סלקטיביות הליגנדים, השליטה, הסלוסטרציה, השינויים שלאחר התרגום והקינטיקה של הקישור ללא גישה לחלבון ולנתונים ביו-פיזיקליים.
למידת מכונה ומחקר דינמיקה מולקולרית מבוסס פיזיקה ניתן לנצל כדי להתגבר על בעיה זו.
חקירות אלו עשויות להפיק תועלת מארכיטקטורת מחשבים מיוחדת ויעילה. בעוד AlphaFold השיגה התקדמות עצומה בחיזוי מבני חלבון, יש עדיין הרבה מה ללמוד בתחום הביולוגיה המבנית, ותחזיות AlphaFold הן רק נקודת ההתחלה למחקר עתידי.
מהם כלים מדהימים אחרים?
RoseTTAFold
RoseTTAFold, שנוצרה על ידי חוקרי אוניברסיטת וושינגטון, משתמשת גם באלגוריתמי למידה עמוקה כדי לחזות מבני חלבון, אך היא גם משלבת גישה חדשה המכונה "סימולציות דינמיות של זווית פיתול" כדי לשפר את המבנים החזויים.
שיטה זו הניבה תוצאות מעודדות ועשויה להיות שימושית בהתגברות על המגבלות של כלי קיפול חלבון AI קיימים.
trRosetta
כלי נוסף, trRosetta, חוזה קיפול חלבון באמצעות א רשת עצבית מאומן על מיליוני רצפים ומבנים של חלבונים.
הוא גם משתמש בטכניקת "דוגמנות מבוססת תבנית" כדי ליצור תחזיות מדויקות יותר על ידי השוואת חלבון המטרה למבנים מוכרים דומים.
הוכח כי trRosetta מסוגלת לחזות את המבנים של חלבונים זעירים ומתחמי חלבון.
DeepMetaPSICOV
DeepMetaPSICOV הוא כלי נוסף המתמקד בחיזוי מפות מגע עם חלבון. אלה, משמשים כמדריך לניבוי קיפול חלבון. זה משתמש למידה עמוקה גישות לחזות את הסבירות לאינטראקציות של שאריות בתוך חלבון.
אלה משמשים לאחר מכן כדי לחזות את מפת הקשר הכוללת. DeepMetaPSICOV הראתה פוטנציאל בחיזוי מבני חלבון בדיוק רב, גם כאשר גישות קודמות נכשלו.
מה צופן העתיד?
העתיד של קיפול חלבון AI הוא בהיר. אלגוריתמים מבוססי למידה עמוקה, בעיקר AlphaFold2, התקדמו לאחרונה בחיזוי אמין של מבני חלבון.
לממצא זה יש פוטנציאל לשנות את פיתוח התרופות בכך שהוא מאפשר למדענים להבין טוב יותר את המבנה והתפקוד של חלבונים, שהם מטרות טיפוליות נפוצות.
עם זאת, נותרו בעיות כמו חיזוי מתחמי חלבון וזיהוי המצב התפקודי האמיתי של מבנים צפויים. נדרש מחקר נוסף כדי לפתור בעיות אלה ולהגביר את הדיוק והאמינות של אלגוריתמים של קיפול חלבון AI.
עם זאת, היתרונות הפוטנציאליים של טכנולוגיה זו הם עצומים, ויש לה פוטנציאל להוביל לייצור תרופות יעילות ומדויקות יותר.





השאירו תגובה