چه می شد اگر بتوانیم از هوش مصنوعی برای پاسخ به یکی از بزرگترین معمای زندگی یعنی تا شدن پروتئین استفاده کنیم؟ دانشمندان ده ها سال است که روی این موضوع کار می کنند.
اکنون ماشینها میتوانند ساختارهای پروتئینی را با دقت شگفتانگیزی با استفاده از مدلهای یادگیری عمیق، تغییر توسعه دارو، بیوتکنولوژی و دانش ما در مورد فرآیندهای بیولوژیکی اساسی پیشبینی کنند.
به من بپیوندید تا در قلمروی جذاب تا شدن پروتئین هوش مصنوعی، جایی که فناوری پیشرفته با پیچیدگی خود زندگی برخورد می کند، به من بپیوندید.
کشف رمز و راز تاخوردگی پروتئین
پروتئین ها در بدن ما مانند ماشین های کوچک برای انجام وظایف حیاتی مانند تجزیه غذا یا انتقال اکسیژن کار می کنند. آنها باید به درستی تا شوند تا بتوانند به طور موثر عمل کنند، درست مانند یک کلید که باید به درستی بریده شود تا در یک قفل قرار گیرد. به محض ایجاد پروتئین، فرآیند تا شدن بسیار پیچیده آغاز می شود.
تاخوردگی پروتئین فرآیندی است که طی آن زنجیرههای طولانی اسیدهای آمینه، بلوکهای سازنده پروتئین، به ساختارهای سهبعدی تا میشوند که عملکرد پروتئین را دیکته میکنند.
یک رشته دراز از مهره ها را در نظر بگیرید که باید به شکل دقیقی سفارش داده شوند. این همان چیزی است که وقتی یک پروتئین تا می شود اتفاق می افتد. با این حال، برخلاف دانهها، اسیدهای آمینه دارای ویژگیهای منحصربهفردی هستند و به روشهای مختلف با یکدیگر تعامل دارند و تاخوردگی پروتئین را به فرآیندی پیچیده و حساس تبدیل میکنند.
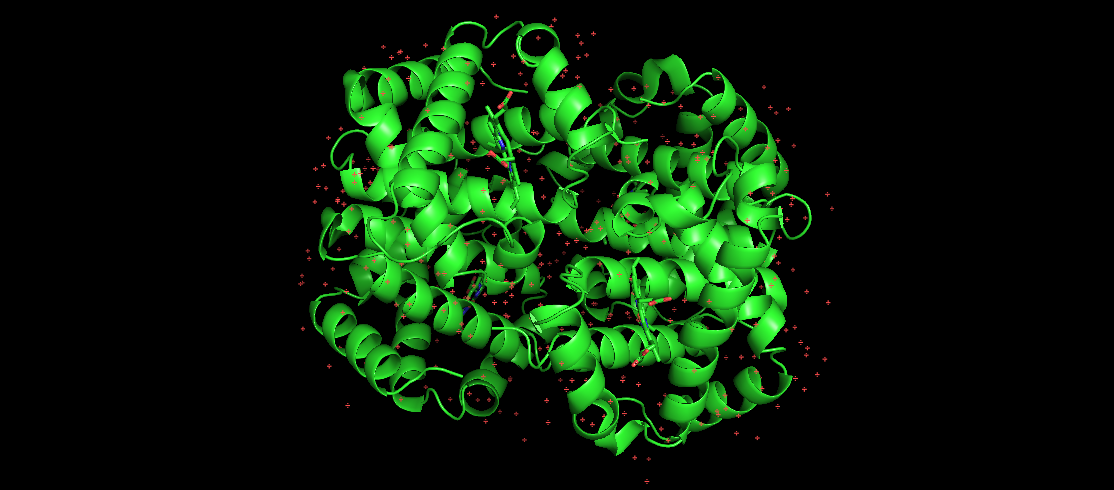
تصویر اینجا نشان دهنده هموگلوبین انسانی است که یک پروتئین چین خورده شناخته شده است
پروتئین ها باید سریع و دقیق تا شوند، در غیر این صورت به اشتباه و معیوب می شوند. این می تواند منجر به بیماری هایی مانند آلزایمر و پارکینسون شود. دما، فشار و حضور سایر مولکولها در سلول، همگی بر فرآیند تا شدن تأثیر میگذارند.
پس از دههها تحقیق، دانشمندان هنوز در تلاشند تا بفهمند پروتئینها دقیقا چگونه تا میشوند.
خوشبختانه، پیشرفت در هوش مصنوعی در حال بهبود توسعه در این بخش است. دانشمندان با استفاده از آن می توانند ساختار پروتئین ها را با دقت بیشتری نسبت به قبل پیش بینی کنند الگوریتم های یادگیری ماشین برای بررسی حجم عظیمی از داده ها
این پتانسیل ایجاد تغییر در توسعه دارو و افزایش دانش مولکولی ما در مورد بیماری را دارد.
آیا ماشین ها می توانند عملکرد بهتری داشته باشند؟
تکنیک های معمولی تا کردن پروتئین دارای محدودیت هایی هستند
دانشمندان ده ها سال است که در تلاش برای کشف تاخوردگی پروتئین بوده اند، اما پیچیدگی این فرآیند این موضوع را به یک موضوع چالش برانگیز تبدیل کرده است.
رویکردهای متداول پیشبینی ساختار پروتئین از ترکیبی از روشهای تجربی و مدلسازی رایانهای استفاده میکنند، با این حال، این روشها همگی دارای اشکالاتی هستند.
تکنیکهای تجربی مانند کریستالوگرافی اشعه ایکس و تشدید مغناطیسی هستهای (NMR) میتوانند زمانبر و پرهزینه باشند. و مدلهای کامپیوتری گاهی اوقات بر فرضیات ساده تکیه میکنند که میتواند منجر به پیشبینیهای اشتباه شود.
هوش مصنوعی می تواند بر این موانع غلبه کند
خوشبختانه، هوش مصنوعی نوید تازه ای برای پیش بینی دقیق تر و کارآمدتر ساختار پروتئین ارائه می دهد. الگوریتم های یادگیری ماشینی می توانند حجم عظیمی از داده ها را بررسی کنند. و الگوهایی را که مردم از دست می دهند را کشف می کنند.
این امر منجر به ایجاد ابزارها و پلتفرم های نرم افزاری جدیدی شده است که قادر به پیش بینی ساختار پروتئین با دقت بی نظیری هستند.
امیدوارکننده ترین الگوریتم های یادگیری ماشین برای پیش بینی ساختار پروتئین
سیستم AlphaFold که توسط گوگل ساخته شده است Deepmind تیم یکی از امیدوار کننده ترین پیشرفت ها در این زمینه است. در سال های اخیر با استفاده از آن پیشرفت زیادی کسب کرده است الگوریتم های یادگیری عمیق برای پیش بینی ساختار پروتئین ها بر اساس توالی اسید آمینه آنها.
شبکههای عصبی، ماشینهای بردار پشتیبان و جنگلهای تصادفی از جمله روشهای یادگیری ماشینی هستند که برای پیشبینی ساختار پروتئین امیدوارکننده هستند.
این الگوریتم ها می توانند از مجموعه داده های عظیم یاد بگیرند. و آنها می توانند همبستگی بین اسیدهای آمینه مختلف را پیش بینی کنند. بنابراین، بیایید ببینیم چگونه کار می کند.

تجزیه و تحلیل های تکاملی و اولین نسل آلفا فولد
موفقیت آلفافولد بر روی یک مدل شبکه عصبی عمیق ساخته شده است که با استفاده از تحلیل هم تکاملی توسعه داده شده است. مفهوم تکامل مشترک بیان می کند که اگر دو اسید آمینه در یک پروتئین با یکدیگر تعامل داشته باشند، با هم توسعه می یابند تا پیوند عملکردی خود را حفظ کنند.
محققان می توانند با مقایسه توالی اسیدهای آمینه چندین پروتئین مشابه، تشخیص دهند که کدام جفت اسید آمینه احتمالاً در ساختار سه بعدی در تماس هستند.
این داده به عنوان پایه ای برای اولین تکرار AlphaFold عمل می کند. طول بین جفت اسیدهای آمینه و همچنین زوایای پیوندهای پپتیدی که آنها را به هم متصل می کند را پیش بینی می کند. این روش از تمام رویکردهای قبلی برای پیشبینی ساختار پروتئین از توالی بهتر عمل کرد، اگرچه دقت برای پروتئینهایی که هیچ الگوی ظاهری نداشتند هنوز محدود بود.

آلفا فولد 2: یک روش کاملاً جدید
AlphaFold2 یک نرم افزار کامپیوتری است که توسط DeepMind ایجاد شده است که از توالی اسید آمینه پروتئین برای پیش بینی ساختار سه بعدی پروتئین استفاده می کند.
این مهم است زیرا ساختار پروتئین نحوه عملکرد آن را دیکته میکند و درک عملکرد آن میتواند به دانشمندان کمک کند داروهایی را بسازند که پروتئین را هدف قرار دهند.
شبکه عصبی AlphaFold2 توالی اسید آمینه پروتئین و همچنین جزئیاتی در مورد نحوه مقایسه آن توالی با سایر توالی های یک پایگاه داده را به عنوان ورودی دریافت می کند (به این ترتیب "تراز توالی" می گویند).
شبکه عصبی بر اساس این ورودی، ساختار سه بعدی پروتئین را پیش بینی می کند.
چه چیزی آن را از AlphaFold2 متمایز می کند؟
برخلاف روشهای دیگر، AlphaFold2 ساختار سهبعدی واقعی پروتئین را پیشبینی میکند نه صرفاً جداسازی بین جفت اسیدهای آمینه یا زوایای بین پیوندهایی که آنها را به هم متصل میکنند (همانطور که الگوریتمهای قبلی انجام میدادند).
برای اینکه شبکه عصبی ساختار کامل را به یکباره پیش بینی کند، ساختار از انتها به انتها کدگذاری می شود.
یکی دیگر از ویژگی های کلیدی AlphaFold2 این است که تخمینی از میزان اطمینان آن در پیش بینی خود ارائه می دهد. این به عنوان یک کدگذاری رنگ در ساختار پیشبینیشده ارائه میشود، که قرمز نشاندهنده اطمینان بالا و آبی نشاندهنده اطمینان کم است.
این مفید است زیرا دانشمندان را در مورد پایداری پیش بینی آگاه می کند.
پیش بینی ساختار ترکیبی چند دنباله
آخرین بسط Alphafold2، معروف به Alphafold Multimer، ساختار ترکیبی چندین توالی را پیشبینی میکند. حتی اگر عملکرد بسیار بهتری نسبت به تکنیک های قبلی داشته باشد، هنوز هم نرخ اشتباه بالایی دارد. فقط 25 درصد از 4500 کمپلکس پروتئینی با موفقیت پیشبینی شد.
70 درصد از مناطق ناهموار تشکیل تماس به درستی پیشبینی شده بودند، اما جهتگیری نسبی دو پروتئین نادرست بود. هنگامی که عمق تراز میانه کمتر از تقریباً 30 دنباله باشد، دقت پیشبینیهای مولتیمر Alphafold به طور قابلتوجهی کاهش مییابد.
نحوه استفاده از پیش بینی های Alphafold
مدلهای پیشبینیشده از AlphaFold در قالبهای فایل مشابهی ارائه میشوند و میتوانند به روشهای مشابه ساختارهای آزمایشی استفاده شوند. برای جلوگیری از سوء تفاهم، مهم است که تخمین های دقت ارائه شده با مدل را در نظر بگیرید.
این به ویژه برای ساختارهای پیچیده مانند هممرهای در هم تنیده یا پروتئین هایی که فقط در حضور یک تا می شوند مفید است.
لیگاند ناشناخته
برخی از چالش ها
مشکل اصلی در استفاده از ساختارهای پیش بینی شده درک دینامیک، انتخاب لیگاند، کنترل، آلوستری، تغییرات پس از ترجمه و سینتیک اتصال بدون دسترسی به پروتئین و داده های بیوفیزیکی است.
فراگیری ماشین و تحقیقات دینامیک مولکولی مبتنی بر فیزیک را می توان برای غلبه بر این مشکل مورد استفاده قرار داد.
این تحقیقات ممکن است از معماری تخصصی و کارآمد کامپیوتر بهره مند شوند. در حالی که AlphaFold به پیشرفت های فوق العاده ای در پیش بینی ساختارهای پروتئین دست یافته است، هنوز چیزهای زیادی برای یادگیری در زمینه زیست شناسی ساختاری وجود دارد، و پیش بینی های AlphaFold تنها نقطه شروع برای مطالعات آینده است.
ابزارهای قابل توجه دیگر چیست؟
RoseTTAFold
RoseTTAFold که توسط محققان دانشگاه واشنگتن ایجاد شده است، به همین ترتیب از الگوریتمهای یادگیری عمیق برای پیشبینی ساختارهای پروتئینی استفاده میکند، اما همچنین رویکرد جدیدی به نام «شبیهسازی دینامیک زاویه پیچشی» را برای بهبود ساختارهای پیشبینیشده ادغام میکند.
این روش نتایج دلگرم کننده ای به همراه داشته است و ممکن است در غلبه بر محدودیت های ابزارهای تاشو پروتئین AI موجود مفید باشد.
trRosetta
ابزار دیگری، trRosetta، تاخوردگی پروتئین را با استفاده از a پیش بینی می کند شبکه های عصبی بر روی میلیون ها توالی و ساختار پروتئینی آموزش دیده است.
همچنین از تکنیک "مدل سازی مبتنی بر الگو" برای ایجاد پیش بینی های دقیق تر با مقایسه پروتئین هدف با ساختارهای شناخته شده قابل مقایسه استفاده می کند.
نشان داده شده است که trRosetta قادر به پیشبینی ساختار پروتئینهای کوچک و کمپلکسهای پروتئینی است.
DeepMetaPSICOV
DeepMetaPSICOV ابزار دیگری است که بر پیش بینی نقشه های تماس پروتئین تمرکز دارد. اینها به عنوان راهنمایی برای پیش بینی تاخوردگی پروتئین استفاده می شوند. استفاده می کند یادگیری عمیق رویکردهایی برای پیشبینی احتمال فعل و انفعالات باقی مانده در یک پروتئین
اینها متعاقباً برای پیشبینی نقشه تماس کلی استفاده میشوند. DeepMetaPSICOV پتانسیل را در پیشبینی ساختارهای پروتئینی با دقت زیادی نشان داده است، حتی زمانی که رویکردهای قبلی شکست خورده باشند.
آینده چه انتظاراتی دارد؟
آینده تاشو پروتئین هوش مصنوعی روشن است. الگوریتمهای مبتنی بر یادگیری عمیق، به ویژه AlphaFold2، اخیراً پیشرفت زیادی در پیشبینی قابل اعتماد ساختارهای پروتئینی داشتهاند.
این یافته این پتانسیل را دارد که توسعه دارو را با اجازه دادن به دانشمندان برای درک بهتر ساختار و عملکرد پروتئین ها، که اهداف درمانی رایج هستند، تغییر دهد.
با این وجود، مسائلی مانند پیشبینی کمپلکسهای پروتئینی و تشخیص وضعیت عملکردی واقعی ساختارهای پیشبینیشده باقی میمانند. تحقیقات بیشتری برای حل این مسائل و افزایش دقت و قابلیت اطمینان الگوریتم های تاشو پروتئین AI مورد نیاز است.
با این حال، مزایای بالقوه این فناوری بسیار زیاد است و این پتانسیل را دارد که منجر به تولید داروهای مؤثرتر و دقیقتر شود.





پاسخ دهید