Was wäre, wenn wir künstliche Intelligenz nutzen könnten, um eines der größten Rätsel des Lebens zu lösen – die Proteinfaltung? Daran arbeiten Wissenschaftler seit Jahrzehnten.
Maschinen können jetzt Proteinstrukturen mit erstaunlicher Präzision vorhersagen, indem sie Deep-Learning-Modelle verwenden, die die Arzneimittelentwicklung, die Biotechnologie und unser Wissen über grundlegende biologische Prozesse verändern.
Begleiten Sie mich auf einer Erkundungstour in das faszinierende Reich der KI-Proteinfaltung, wo Spitzentechnologie mit der Komplexität des Lebens selbst kollidiert.
Das Geheimnis der Proteinfaltung lüften
Proteine arbeiten in unserem Körper wie kleine Maschinen, die entscheidende Aufgaben wie den Abbau von Nahrung oder den Transport von Sauerstoff übernehmen. Sie müssen richtig gefaltet werden, damit sie effektiv funktionieren, genau wie ein Schlüssel richtig geschnitten werden muss, damit er in ein Schloss passt. Sobald das Protein entsteht, beginnt ein sehr komplizierter Faltungsprozess.
Proteinfaltung ist der Prozess, bei dem sich lange Aminosäureketten, die Bausteine des Proteins, zu dreidimensionalen Strukturen falten, die die Funktion des Proteins bestimmen.
Stellen Sie sich eine lange Perlenkette vor, die in eine präzise Form gebracht werden muss; Das passiert, wenn sich ein Protein faltet. Im Gegensatz zu Perlen haben Aminosäuren jedoch einzigartige Eigenschaften und interagieren auf verschiedene Weise miteinander, was die Proteinfaltung zu einem komplexen und empfindlichen Prozess macht.
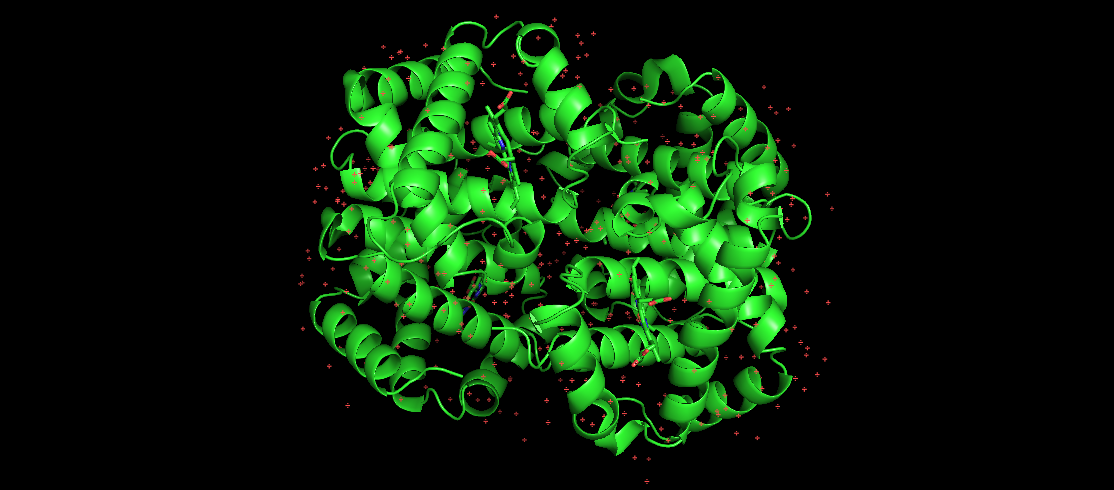
Das Bild hier zeigt menschliches Hämoglobin, ein bekanntes gefaltetes Protein
Proteine müssen sich schnell und präzise falten, sonst werden sie falsch gefaltet und defekt. Das könnte zu Krankheiten wie Alzheimer und Parkinson führen. Temperatur, Druck und das Vorhandensein anderer Moleküle in der Zelle wirken sich alle auf den Faltungsprozess aus.
Nach jahrzehntelanger Forschung versuchen Wissenschaftler immer noch herauszufinden, wie sich Proteine genau falten.
Glücklicherweise verbessern Fortschritte in der künstlichen Intelligenz die Entwicklung in der Branche. Mit Hilfe von können Wissenschaftler die Struktur von Proteinen genauer als je zuvor vorhersagen Algorithmen für maschinelles Lernen große Datenmengen zu untersuchen.
Dies hat das Potenzial, die Medikamentenentwicklung zu verändern und unser molekulares Wissen über die Krankheit zu erweitern.
Können Maschinen mehr leisten?
Herkömmliche Techniken zur Proteinfaltung haben Einschränkungen
Wissenschaftler versuchen seit Jahrzehnten, die Proteinfaltung zu verstehen, aber die Kompliziertheit des Prozesses hat dies zu einem herausfordernden Thema gemacht.
Herkömmliche Ansätze zur Proteinstrukturvorhersage verwenden eine Kombination aus experimentellen Methoden und Computermodellierung, jedoch haben diese Methoden alle Nachteile.
Experimentelle Techniken wie Röntgenkristallographie und Kernspinresonanz (NMR) können zeitaufwändig und kostspielig sein. Und Computermodelle beruhen manchmal auf einfachen Annahmen, was zu fehlerhaften Vorhersagen führen kann.
KI kann diese Hindernisse überwinden
Zum Glück künstliche Intelligenz bietet ein neues Versprechen für eine genauere und effizientere Vorhersage der Proteinstruktur. Algorithmen für maschinelles Lernen können riesige Datenmengen untersuchen. Und sie decken Muster auf, die Menschen übersehen würden.
Dies hat zur Entwicklung neuer Softwaretools und Plattformen geführt, die in der Lage sind, die Proteinstruktur mit beispielloser Präzision vorherzusagen.
Die vielversprechendsten maschinellen Lernalgorithmen für die Proteinstrukturvorhersage
Das von Google entwickelte AlphaFold-System DeepMind team ist einer der vielversprechendsten Fortschritte in diesem Bereich. Es hat in den letzten Jahren durch die Verwendung große Fortschritte gemacht Deep-Learning-Algorithmen um die Struktur von Proteinen anhand ihrer Aminosäuresequenzen vorherzusagen.
Neuronale Netze, Support Vector Machines und Random Forests gehören zu weiteren Methoden des maschinellen Lernens, die für die Vorhersage der Proteinstruktur vielversprechend sind.
Diese Algorithmen können aus riesigen Datensätzen lernen. Und sie können die Korrelationen zwischen verschiedenen Aminosäuren antizipieren. Mal sehen, wie es funktioniert.

Koevolutionäre Analysen und die erste AlphaFold-Generation
Der Erfolg AlphaFold basiert auf einem tiefen neuronalen Netzwerkmodell, das mithilfe koevolutionärer Analyse entwickelt wurde. Das Konzept der Co-Evolution besagt, dass wenn zwei Aminosäuren in einem Protein miteinander interagieren, sie sich gemeinsam entwickeln, um ihre funktionelle Verbindung aufrechtzuerhalten.
Forscher können erkennen, welche Aminosäurepaare in der 3D-Struktur wahrscheinlich in Kontakt stehen, indem sie die Aminosäuresequenzen zahlreicher ähnlicher Proteine vergleichen.
Diese Daten dienen als Grundlage für die erste Iteration von AlphaFold. Es sagt die Längen zwischen Aminosäurepaaren sowie die Winkel der Peptidbindungen voraus, die sie verbinden. Dieses Verfahren übertraf alle früheren Ansätze zur Vorhersage der Proteinstruktur aus der Sequenz, obwohl die Genauigkeit für Proteine ohne offensichtliche Vorlagen immer noch eingeschränkt war.

AlphaFold 2: Eine radikal neue Methodik
AlphaFold2 ist eine von DeepMind entwickelte Computersoftware, die die Aminosäuresequenz eines Proteins verwendet, um die 3D-Struktur des Proteins vorherzusagen.
Dies ist von Bedeutung, da die Struktur eines Proteins seine Funktionsweise bestimmt und das Verständnis seiner Funktion Wissenschaftlern helfen kann, Medikamente zu entwickeln, die auf das Protein abzielen.
Das neuronale AlphaFold2-Netzwerk erhält als Eingabe die Aminosäuresequenz des Proteins sowie Details darüber, wie diese Sequenz im Vergleich zu anderen Sequenzen in einer Datenbank abschneidet (dies wird als „Sequenzabgleich“ bezeichnet).
Das neuronale Netzwerk trifft anhand dieser Eingabe eine Vorhersage über die 3D-Struktur des Proteins.
Was unterscheidet es von AlphaFold2?
Im Gegensatz zu anderen Ansätzen sagt AlphaFold2 die echte 3D-Struktur des Proteins voraus und nicht nur die Trennung zwischen Aminosäurepaaren oder die Winkel zwischen den sie verbindenden Bindungen (wie es frühere Algorithmen taten).
Damit das neuronale Netzwerk sofort die vollständige Struktur antizipieren kann, wird die Struktur Ende-zu-Ende codiert.
Ein weiteres wichtiges Merkmal von AlphaFold2 ist, dass es eine Schätzung darüber bietet, wie sicher es in seiner Prognose ist. Dies wird als Farbcodierung der erwarteten Struktur dargestellt, wobei Rot für hohes Vertrauen und Blau für geringes Vertrauen steht.
Dies ist nützlich, da es Wissenschaftler über die Stabilität der Vorhersage informiert.
Vorhersage der kombinierten Struktur mehrerer Sequenzen
Die neueste Erweiterung von Alphafold2, bekannt als Alphafold Multimer, prognostiziert die kombinierte Struktur mehrerer Sequenzen. Es hat immer noch hohe Fehlerquoten, auch wenn es weitaus besser abschneidet als frühere Techniken. Nur 25 % von 4500 Proteinkomplexen wurden erfolgreich vorhergesagt.
70 % der groben Bereiche der Kontaktbildung wurden richtig vorhergesagt, aber die relative Orientierung der beiden Proteine war falsch. Wenn die mittlere Ausrichtungstiefe weniger als etwa 30 Sequenzen beträgt, nimmt die Genauigkeit der Alphafold-Multimer-Vorhersagen erheblich ab.
So verwenden Sie Alphafold-Vorhersagen
Die vorhergesagten Modelle von AlphaFold werden in den gleichen Dateiformaten angeboten und können auf die gleiche Weise wie experimentelle Strukturen verwendet werden. Es ist wichtig, die mit dem Modell angebotenen Genauigkeitsschätzungen zu berücksichtigen, um Missverständnisse zu vermeiden.
Es ist besonders hilfreich bei komplizierten Strukturen wie verwobenen Homomeren oder Proteinen, die sich nur in Gegenwart von falten
unbekannter Ligand.
Einige Herausforderungen
Das Hauptproblem bei der Verwendung vorhergesagter Strukturen ist das Verständnis der Dynamik, Ligandenselektivität, Kontrolle, Allosterie, posttranslationalen Veränderungen und Bindungskinetik ohne Zugang zu Protein- und biophysikalischen Daten.
Maschinelles Lernen und physikbasierte Molekulardynamikforschung kann genutzt werden, um dieses Problem zu überwinden.
Diese Untersuchungen können von einer spezialisierten und effizienten Computerarchitektur profitieren. Während AlphaFold enorme Fortschritte bei der Vorhersage von Proteinstrukturen erzielt hat, gibt es auf dem Gebiet der Strukturbiologie noch viel zu lernen, und AlphaFold-Vorhersagen sind nur der Ausgangspunkt für zukünftige Studien.
Was sind andere bemerkenswerte Tools?
RoseTTAFold
RoseTTAFold, das von Forschern der University of Washington entwickelt wurde, verwendet ebenfalls Deep-Learning-Algorithmen zur Vorhersage von Proteinstrukturen, integriert aber auch einen neuartigen Ansatz, der als „Torsionswinkel-Dynamik-Simulationen“ bekannt ist, um die vorhergesagten Strukturen zu verbessern.
Diese Methode hat ermutigende Ergebnisse geliefert und kann nützlich sein, um die Einschränkungen bestehender AI-Proteinfaltungswerkzeuge zu überwinden.
trRosetta
Ein weiteres Tool, trRosetta, sagt die Proteinfaltung mithilfe von a voraus neuronale Netzwerk an Millionen von Proteinsequenzen und -strukturen trainiert.
Es verwendet auch eine Technik der „schablonenbasierten Modellierung“, um genauere Vorhersagen zu treffen, indem das Zielprotein mit vergleichbaren bekannten Strukturen verglichen wird.
Es wurde gezeigt, dass trRosetta in der Lage ist, die Strukturen von winzigen Proteinen und Proteinkomplexen vorherzusagen.
DeepMetaPSICOV
DeepMetaPSICOV ist ein weiteres Tool, das sich auf die Vorhersage von Proteinkontaktkarten konzentriert. Diese werden als Richtlinie zur Vorhersage der Proteinfaltung verwendet. Es benutzt tiefe Lernen Ansätze zur Vorhersage der Wahrscheinlichkeit von Aminosäurewechselwirkungen innerhalb eines Proteins.
Diese werden anschließend verwendet, um die gesamte Kontaktkarte zu prognostizieren. DeepMetaPSICOV hat das Potenzial gezeigt, Proteinstrukturen mit großer Genauigkeit vorherzusagen, selbst wenn frühere Ansätze gescheitert sind.
Was hält die Zukunft bereit?
Die Zukunft der KI-Proteinfaltung ist rosig. Deep-Learning-basierte Algorithmen, insbesondere AlphaFold2, haben in letzter Zeit große Fortschritte bei der zuverlässigen Vorhersage von Proteinstrukturen gemacht.
Diese Erkenntnis hat das Potenzial, die Arzneimittelentwicklung zu verändern, indem sie es Wissenschaftlern ermöglicht, die Struktur und Funktion von Proteinen, die häufig therapeutische Ziele sind, besser zu verstehen.
Dennoch bleiben Probleme wie die Vorhersage von Proteinkomplexen und die Erkennung des tatsächlichen funktionellen Status erwarteter Strukturen bestehen. Weitere Forschung ist erforderlich, um diese Probleme zu lösen und die Genauigkeit und Zuverlässigkeit von AI-Proteinfaltungsalgorithmen zu erhöhen.
Die potenziellen Vorteile dieser Technologie sind jedoch enorm, und sie hat das Potenzial, zur Herstellung wirksamerer und präziserer Medikamente zu führen.





Hinterlassen Sie uns einen Kommentar