ماذا لو تمكنا من استخدام الذكاء الاصطناعي للإجابة على أحد أعظم ألغاز الحياة - طي البروتين؟ يعمل العلماء على هذا منذ عقود.
يمكن للآلات الآن التنبؤ بهياكل البروتين بدقة مذهلة باستخدام نماذج التعلم العميق ، وتغيير تطوير الأدوية ، والتكنولوجيا الحيوية ، ومعرفتنا بالعمليات البيولوجية الأساسية.
انضم إلي لاستكشاف عالم مثير للاهتمام لطي البروتين بالذكاء الاصطناعي ، حيث تصطدم التكنولوجيا المتطورة مع تعقيد الحياة نفسها.
كشف لغز طي البروتين
تعمل البروتينات في أجسامنا مثل الآلات الصغيرة للقيام بمهام حاسمة مثل تكسير الطعام أو نقل الأكسجين. يجب طيها بشكل صحيح حتى تعمل بشكل فعال ، تمامًا مثل قطع المفتاح بشكل صحيح ليناسب القفل. بمجرد تكوين البروتين ، تبدأ عملية طي معقدة للغاية.
طي البروتين هو العملية التي يتم من خلالها طي السلاسل الطويلة من الأحماض الأمينية ، اللبنات الأساسية للبروتين ، إلى هياكل ثلاثية الأبعاد تملي وظيفة البروتين.
ضع في اعتبارك سلسلة طويلة من الخرزات التي يجب ترتيبها في شكل دقيق ؛ هذا ما يحدث عندما ينثني البروتين. ومع ذلك ، على عكس الخرز ، تتمتع الأحماض الأمينية بخصائص فريدة وتتفاعل مع بعضها البعض بطرق مختلفة ، مما يجعل طي البروتين عملية معقدة وحساسة.
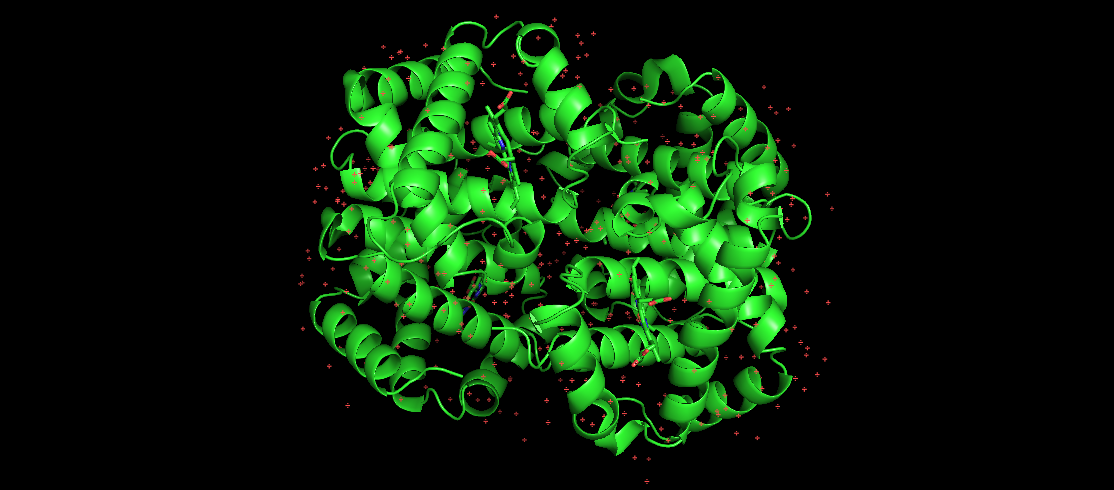
تمثل الصورة هنا الهيموجلوبين البشري ، وهو بروتين مطوي معروف جيدًا
يجب أن تطوى البروتينات بسرعة وبدقة ، وإلا فإنها ستصبح معيبة ومعيبة. يمكن أن يؤدي ذلك إلى أمراض مثل مرض الزهايمر وباركنسون. تؤثر درجة الحرارة والضغط ووجود جزيئات أخرى في الخلية على عملية الطي.
بعد عقود من البحث ، لا يزال العلماء يحاولون معرفة بالضبط كيف تنطوى البروتينات.
لحسن الحظ ، تعمل التطورات في مجال الذكاء الاصطناعي على تحسين التنمية في هذا القطاع. يمكن للعلماء توقع بنية البروتينات بشكل أكثر دقة من أي وقت مضى باستخدامها خوارزميات التعلم الآلي لفحص كميات هائلة من البيانات.
هذا لديه القدرة على تغيير تطوير الأدوية وزيادة معرفتنا الجزيئية للمرض.
هل يمكن للآلات أن تعمل بشكل أفضل؟
تقنيات الطي بالبروتين التقليدية لها حدود
يحاول العلماء اكتشاف إمكانية طي البروتين لعقود من الزمن ، لكن تعقيد العملية جعل هذا الموضوع صعبًا.
تستخدم مناهج التنبؤ ببنية البروتين التقليدية مزيجًا من المنهجيات التجريبية ونمذجة الكمبيوتر ، ومع ذلك ، فإن هذه الطرق جميعها لها عيوب.
يمكن أن تكون التقنيات التجريبية مثل علم البلورات بالأشعة السينية والرنين المغناطيسي النووي (NMR) مضيعة للوقت ومكلفة. وتعتمد نماذج الكمبيوتر أحيانًا على افتراضات بسيطة ، مما قد يؤدي إلى تنبؤات خاطئة.
يمكن للذكاء الاصطناعي التغلب على هذه العقبات
لحسن الحظ، الذكاء الاصطناعي يقدم وعدًا جديدًا لتوقع بنية بروتينية أكثر دقة وكفاءة. يمكن لخوارزميات التعلم الآلي فحص كميات هائلة من البيانات. ويكشفون عن أنماط قد يفوتها الناس.
وقد أدى ذلك إلى إنشاء أدوات ومنصات برمجية جديدة قادرة على التنبؤ بهيكل البروتين بدقة لا مثيل لها.
أكثر خوارزميات التعلم الآلي الواعدة للتنبؤ بهيكل البروتين
نظام AlphaFold الذي أنشأته شركة Google العقل العميق يعد فريق العمل أحد أكثر التطورات الواعدة في هذا المجال. لقد اكتسبت تقدمًا كبيرًا في السنوات الأخيرة باستخدام خوارزميات التعلم العميق للتنبؤ ببنية البروتينات بناءً على تسلسل الأحماض الأمينية الخاصة بها.
تعد الشبكات العصبية وآلات ناقلات الدعم والغابات العشوائية من بين المزيد من أساليب التعلم الآلي التي تبشر بتوقع بنية البروتين.
يمكن أن تتعلم هذه الخوارزميات من مجموعات البيانات الهائلة. ويمكنهم توقع العلاقات المتبادلة بين الأحماض الأمينية المختلفة. لذلك ، دعونا نرى كيف يعمل.

التحليلات التطورية المشتركة وجيل AlphaFold الأول
نجاح AlphaFold مبني على نموذج شبكة عصبية عميقة تم تطويره باستخدام التحليل التطوري المشترك. ينص مفهوم التطور المشترك على أنه إذا تفاعل اثنان من الأحماض الأمينية في البروتين مع بعضهما البعض ، فسوف يتطوران معًا للحفاظ على ارتباطهما الوظيفي.
يمكن للباحثين اكتشاف أزواج الأحماض الأمينية التي من المحتمل أن تكون على اتصال في البنية ثلاثية الأبعاد من خلال مقارنة تسلسل الأحماض الأمينية للعديد من البروتينات المماثلة.
تعمل هذه البيانات كأساس للتكرار الأول لـ AlphaFold. يتنبأ بالأطوال بين أزواج الأحماض الأمينية وكذلك زوايا روابط الببتيد التي تربطهم. تفوقت هذه الطريقة على جميع الأساليب السابقة للتنبؤ ببنية البروتين من التسلسل ، على الرغم من أن الدقة كانت لا تزال مقيدة بالنسبة للبروتينات التي لا تحتوي على قوالب ظاهرة.

AlphaFold 2: منهجية جديدة جذريًا
AlphaFold2 هو برنامج كمبيوتر تم إنشاؤه بواسطة DeepMind يستخدم تسلسل الأحماض الأمينية للبروتين للتنبؤ بالبنية ثلاثية الأبعاد للبروتين.
هذا مهم لأن بنية البروتين تحدد كيفية عمله ، وفهم وظيفته يمكن أن يساعد العلماء على تطوير الأدوية التي تستهدف البروتين.
تستقبل الشبكة العصبية AlphaFold2 كمدخلات تسلسل الأحماض الأمينية للبروتين بالإضافة إلى تفاصيل حول كيفية مقارنة هذا التسلسل بالتسلسلات الأخرى في قاعدة البيانات (وهذا ما يسمى "محاذاة التسلسل").
تقوم الشبكة العصبية بعمل تنبؤ حول بنية البروتين ثلاثية الأبعاد بناءً على هذه المدخلات.
ما الذي يميزه عن AlphaFold2؟
على عكس الأساليب الأخرى ، يتنبأ AlphaFold2 بالبنية ثلاثية الأبعاد الحقيقية للبروتين بدلاً من مجرد الفصل بين أزواج الأحماض الأمينية أو الزوايا بين الروابط التي تربطها (كما فعلت الخوارزميات السابقة).
من أجل أن تتوقع الشبكة العصبية البنية الكاملة في وقت واحد ، يتم ترميز البنية من طرف إلى طرف.
السمة الرئيسية الأخرى لـ AlphaFold2 هي أنها تقدم تقديرًا لمدى ثقتها في توقعاتها. يتم تقديم هذا على شكل ترميز لوني على الهيكل المتوقع ، حيث يمثل اللون الأحمر ثقة عالية بينما يشير اللون الأزرق إلى ثقة منخفضة.
هذا مفيد لأنه يخبر العلماء عن ثبات التنبؤ.
توقع البنية المدمجة لعدة متواليات
أحدث توسع لـ Alphafold2 ، المعروف باسم Alphafold Multimer ، يتنبأ بالبنية المدمجة لعدة متواليات. لا يزال لديها معدلات أخطاء عالية حتى لو كان أداؤها أفضل بكثير من التقنيات السابقة. تم توقع 25 ٪ فقط من 4500 مجمع بروتيني بنجاح.
تم التنبؤ بشكل صحيح بـ 70٪ من المناطق الخشنة لتكوين التلامس ، لكن الاتجاه النسبي للبروتينين كان غير صحيح. عندما يكون متوسط عمق المحاذاة أقل من 30 تسلسلًا تقريبًا ، تنخفض دقة تنبؤات Alphafold المتعددة بشكل كبير.
كيفية استخدام تنبؤات Alphafold
يتم تقديم النماذج المتوقعة من AlphaFold بنفس تنسيقات الملفات ويمكن استخدامها بنفس الطرق مثل الهياكل التجريبية. من الأهمية بمكان مراعاة تقديرات الدقة المقدمة مع النموذج من أجل منع سوء الفهم.
إنه مفيد بشكل خاص للهياكل المعقدة مثل المتجانسات المتشابكة أو البروتينات التي تنثني فقط في وجود
يجند غير معروف.
بعض التحديات
تكمن المشكلة الرئيسية في استخدام الهياكل المتوقعة في فهم الديناميكيات وانتقائية الترابط والتحكم والتماثل والتغييرات اللاحقة للترجمة وحركية الارتباط دون الوصول إلى البيانات البروتينية والفيزيائية الحيوية.
تعلم الآلة ويمكن استخدام أبحاث الديناميكيات الجزيئية القائمة على الفيزياء للتغلب على هذه المشكلة.
قد تستفيد هذه التحقيقات من هندسة الكمبيوتر المتخصصة والفعالة. بينما حقق AlphaFold تقدمًا هائلاً في التنبؤ بهياكل البروتين ، لا يزال هناك الكثير لنتعلمه في مجال البيولوجيا الهيكلية ، وتنبؤات AlphaFold ليست سوى نقطة البداية للدراسة المستقبلية.
ما هي الأدوات الأخرى الرائعة؟
روز تافولد
يستخدم RoseTTAFold ، الذي أنشأه باحثو جامعة واشنطن ، أيضًا خوارزميات التعلم العميق للتنبؤ بهياكل البروتين ، ولكنه يدمج أيضًا نهجًا جديدًا يُعرف باسم "محاكاة ديناميات زاوية الالتواء" لتحسين الهياكل المتوقعة.
لقد أسفرت هذه الطريقة عن نتائج مشجعة وقد تكون مفيدة في التغلب على قيود أدوات طي البروتين الموجودة في الذكاء الاصطناعي.
trروزيتا
تتنبأ أداة أخرى ، TrRosetta ، بطي البروتين باستخدام أ الشبكة العصبية تم تدريبه على الملايين من سلاسل البروتينات وهياكلها.
كما أنها تستخدم تقنية "النمذجة القائمة على القالب" لإنشاء تنبؤات أكثر دقة من خلال مقارنة البروتين المستهدف بالتركيبات المعروفة المماثلة.
لقد ثبت أن trRosetta قادرة على التنبؤ بهياكل البروتينات الدقيقة ومجمعات البروتين.
ديب ميتابسيكوف
DeepMetaPSICOV هي أداة أخرى تركز على التنبؤ بخرائط اتصال البروتين. تستخدم هذه كدليل للتنبؤ بطي البروتين. يستخدم التعلم العميق نهج للتنبؤ باحتمالية تفاعلات المخلفات داخل البروتين.
يتم استخدام هذه لاحقًا للتنبؤ بخريطة الاتصال الشاملة. أظهر DeepMetaPSICOV إمكانية التنبؤ بهياكل البروتين بدقة كبيرة ، حتى عندما فشلت الأساليب السابقة.
ماذا يحمل المستقبل؟
مستقبل طي البروتين بالذكاء الاصطناعي مشرق. حققت الخوارزميات القائمة على التعلم العميق ، ولا سيما AlphaFold2 ، تقدمًا كبيرًا مؤخرًا في التنبؤ الموثوق به لهياكل البروتين.
هذا الاكتشاف لديه القدرة على تحويل تطوير الأدوية من خلال السماح للعلماء بفهم أفضل لبنية ووظيفة البروتينات ، وهي أهداف علاجية شائعة.
ومع ذلك ، لا تزال هناك مشكلات مثل التنبؤ بمجمعات البروتين واكتشاف الحالة الوظيفية الحقيقية للهياكل المتوقعة. هناك حاجة إلى مزيد من البحث لحل هذه المشكلات وزيادة دقة وموثوقية خوارزميات طي البروتين بالذكاء الاصطناعي.
ومع ذلك ، فإن الفوائد المحتملة لهذه التكنولوجيا هائلة ، ولديها القدرة على أن تؤدي إلى إنتاج أدوية أكثر فعالية ودقة.





اترك تعليق